
【題目】下列離子方程式正確的是
A.碳酸鈣與醋酸反應:CaCO3+2H+=Ca2++H2O+CO2↑
B.鐵與氯化鐵溶液反應:Fe+Fe3+=2Fe2+
C.碳酸氫鈉溶液與氫氧化鈉溶液混合:HCO3-+OH-=H2O+CO2↑
D.將氯氣通入KBr溶液中:Cl2+2Br-=2Cl-+Br2
 心算口算巧算一課一練系列答案
心算口算巧算一課一練系列答案科目:高中化學 來源: 題型:
【題目】一定條件下,在容積不變的密閉容器中加入P、Q進行反應P(g)+2Q(g)![]() 3R(g)+S(l),說明該反應達到平衡的是
3R(g)+S(l),說明該反應達到平衡的是
A.反應容器中氣體的平均摩爾質量不再改變
B.反應容器中P、Q、R、S四者共存
C.2v正(Q)=3 v逆(R)
D.反應容器中壓強不隨時間變化而變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是某化學研究小組探究外界條件對化學反應速率和化學平衡影響的圖像,其中圖像和實驗結論表達均正確的是

A. ①是其它條件一定時,反應速率隨溫度變化的圖象,正反應△H<0
B. ②是在平衡體系的溶液中溶入少量KCl晶體后化學反應速率隨時間變化的圖像
C. ③是在有無催化劑存在下建立的平衡過程圖象,曲線a是使用催化劑的曲線
D. ④是一定條件下,向含有一定量A的容器中逐漸加入B時的圖象,壓強p1>p2
查看答案和解析>>
科目:高中化學 來源: 題型:
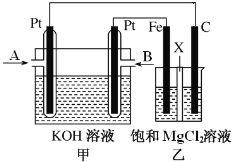
【題目】下圖中甲為甲烷和O2構成的燃料電池示意圖,電解質為KOH溶液,乙為電解飽和MgCl2溶液的裝置,其中乙裝置中X為陽離子交換膜。用該裝置進行實驗,反應開始后觀察到Fe電極附近出現白色沉淀。下列說法正確的是
A.甲中A處通入CH4,電極反應式為CH4+10OH8e![]() +7H2O
+7H2O
B.乙中電解MgCl2溶液的總反應為2Cl+2H2O![]() Cl2↑+H2↑+2OH
Cl2↑+H2↑+2OH
C.理論上甲中每消耗22.4 L CH4(標準狀況下),乙中產生4 mol Cl2
D.甲、乙中電解質溶液的pH都增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有Na+、Mg2+、Fe2+、H+、HCO3-、OH-、Cl-、NO3-、I-中的若干種,向該溶液中加入鋁粉后,溶液中有AlO2-生成,則原溶液中能大最共存的離子最多有
A. 4種 B. 5種 C. 6種 D. 7種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向體積為2 L的密閉容器中充入2 mol SO2和1 mol O2,測得起始容器壓強為p,一定條件下發生反應:2SO2(g)+O2(g)![]() 2SO3(g) △H=-196 kJ·mol-1,維持容器溫度不變,測得平衡時容器內壓強為0.7p,若此時再向容器中充入2 mol SO3,則下列說法正確的是
2SO3(g) △H=-196 kJ·mol-1,維持容器溫度不變,測得平衡時容器內壓強為0.7p,若此時再向容器中充入2 mol SO3,則下列說法正確的是
A. 充入2 mol SO3后,SO2的物質的量增大
B. 第一次反應達到平衡時共放出熱量176.4 kJ
C. 充入2 mol SO3達到新平衡時,容器內的壓強為1.4p
D. 降低容器的溫度可使新平衡時各物質的體積分數與第一次平衡時相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硝酸生產中,500℃時,NH3和O2可能發生如下反應:
① 4NH3 (g) + 5O2 (g) ![]() 4NO (g) + 6H2O (g) △H= - 9072 kJ·mol-1K= 1.1×1026
4NO (g) + 6H2O (g) △H= - 9072 kJ·mol-1K= 1.1×1026
② 4NH3 (g) + 4O2 (g) ![]() 2N2O (g) + 6H2O (g) △H= - 1105 kJ·mol-1K= 4.4×1028
2N2O (g) + 6H2O (g) △H= - 1105 kJ·mol-1K= 4.4×1028
③ 4NH3 (g) + 3O2 (g) ![]() 2N2 (g) + 6H2O (g) △H= - 1269 kJ·mol-1K= 7.1×1034
2N2 (g) + 6H2O (g) △H= - 1269 kJ·mol-1K= 7.1×1034
其中,②、③是副反應。若要減少副反應,提高NO的產率,最合理的措施是
A.減小壓強 B.降低溫度
C.增大O2濃度 D.使用合適的催化劑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com