
【題目】根據你對金屬鈉性質的了解,回答下列問題:
(1)關于鈉的敘述中,正確的是________(填字母)。
A.鈉是銀白色金屬,硬度很大
B.將金屬鈉放在石棉網上,用酒精燈加熱后金屬鈉劇烈燃燒,產生黃色火焰,生成過氧化鈉
C.金屬鈉在空氣中燃燒,生成氧化鈉
D.金屬鈉的熔點很高
(2)由于金屬鈉很容易跟空氣中的______、________等物質反應,通常將它保存在_______里。
(3)將一小塊鈉投入到下列溶液中,既能產生氣體又會出現白色沉淀的是________(填字母)。
A.稀硫酸 B.硫酸銅溶液
C.氫氧化鈉溶液 D.氯化鎂溶液
(4)為粗略測定金屬鈉的相對原子質量,設計的裝置如圖所示,該裝置(包括水)的總質量為ag,將質量為bg的鈉(不足量)放入水中,立即塞緊瓶塞。完全反應后再稱量此裝置的總質量為cg。
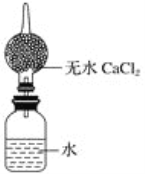
①列出計算鈉相對原子質量的數學表達式______________(用含有a、b、c的算式表示)。
②無水氯化鈣的作用是____________________。
【答案】B 氧氣 水蒸氣 煤油 D b/(a+b-c) 吸收H2中所含的H2O(g)
【解析】
(1)根據鈉的性質分析解答;
(2)鈉的性質很活潑,易和水、氧氣反應,據此解答;
(3)金屬鈉投入水中生成氫氧化鈉和氫氣,根據溶液中的溶質分析解答;
(4)①根據鈉與水反應產生氫氣的質量關系以及反應前后質量差解答;
②根據產生的氣體中含有水蒸氣分析判斷。
(1)A、鈉是銀白色金屬,硬度很小,可以用小刀切,故A錯誤;
B、鈉在空氣中燃燒產物是淡黃色的過氧化鈉,故B正確;
C、鈉在空氣中燃燒產物是淡黃色的過氧化鈉,不是氧化鈉,故C錯誤;
D、金屬鈉的熔點很低,故D錯誤;
故答案選B;
(2)鈉性質很活潑,易和水、氧氣反應,所以保存鈉時要隔絕空氣和水,鈉和煤油不反應,且密度大于煤油,所以保存鈉可以放在煤油中;
(3)A.鈉和稀硫酸反應生成硫酸鈉和氫氣,沒有沉淀產生,A不選;
B.鈉投入硫酸銅溶液中,首先和水反應生成氫氧化鈉和氫氣,氫氧化鈉和硫酸銅反應生成氫氧化銅沉淀和硫酸鈉,但沉淀不是白色的,而是藍色的,B不選;
C.鈉投入氫氧化鈉溶液中生成氫氧化鈉和氫氣,沒有沉淀,C不選;
D.鈉投入氯化鎂溶液中生成氯化鈉、氫氧化鎂白色沉淀和氫氣,D選。
答案選D。
(4)①金屬與水發生反應放出氫氣的質量=ag+bg-cg=(a+b-c)g,假設金屬為R,其相對原子質量為M,根據金屬鈉與水反應放出氫氣的關系,可推斷該金屬與水放出氫氣關系如下:
2R~~~~~H2
2M 2
bg (a+b-c)g
解得M=b/(a+b-c);
②氯化鈣具有吸水能力,是常用的干燥劑,在裝置中吸收生成氫氣中的水,而防止水分流失。


科目:高中化學 來源: 題型:
【題目】自來水常用氯氣消毒,某學生用這種自來水去配制下列物質溶液,不會產生明顯的藥品變質問題的是 ( )
A. AgNO3 B. FeCl2
C. NaHSO3 D. NaNO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】次磷酸鈷[Co(H2PO2)2·6H2O]可用于化學電鍍,共飽和溶液的pH約為6;利用電滲析法可在產品室析出高純[Co(H2PO2)2·6H2O]電滲析原理如圖所示。則陽離子交換膜有
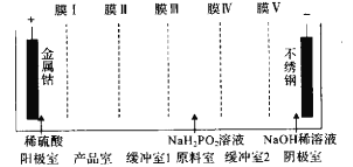
A. 1個 B. 2個 C. 3個 D. 4個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素W、X、Y、Z的原子序數依次增大:W、X、Y、Z組成的單質可發生如圖所示的化學反應;B是生活中最常見的液體;常溫下Y、Z組成的二元化合物的水溶液pH=7。下列說法錯誤的是
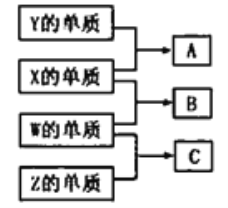
A. A與B的反應一定是化合反應
B. 離子半徑:Z>X>Y>W
C. W、Y、Z均存在兩種或兩種以上的氧化物
D. 將等物質的量的A、C溶于同一燒杯水中,所得溶液的pH一定大于7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)若某原子在處于能最最低狀態時,外圍電子排布為4d15s2,則下列說法正確的是___(填標號)
A.該元戴原子處于能量最低狀態時,原子中共有3個未成對電子
B.該元載原子核外共有5個電子層
C.該元素原子的M能層共有8個電子
D.該元素原子最外層其有3個電子
(2)下列說法正確的是_______(填標號)
A.共價鍵的鍵能越大,共價鍵越牢固,由該鍵形成的分子越穩定
B.H2O是一種非常穩定的化合物,這是由于氫鍵所致
C.H2O分子中兩個O-H鍵的鍵角為180°
D.所有分子中都含有共價鍵
(3)根據價層電子對互斥理論及原子的雜化理論判斷NF3分子的空間構型和中心原子的雜化方式為____(填標號)
A.直線形 sp雜化 B.三角形 sp2雜化
C.三角錐形 sp2雜化 D.三角錐形 sp3雜化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤炭燃燒過程中會釋放出大量的SO2,嚴重破壞生態環境。采用一定的脫硫技術可以把硫元素以CaSO4的形式固定,從而降低SO2的排放。但是煤炭燃燒過程中產生的CO又會與CaSO4發生化學反應,降低脫硫效率。相關反應的熱化學方程式如下:
CaSO4(s)+CO(g) CaO(s) + SO2(g) + CO2(g) ΔH1=+218.4kJ·mol-1(反應Ⅰ)
CaSO4(s)+4CO(g) CaS(s) + 4CO2(g) ΔH2= -175.6kJ·mol-1(反應Ⅱ)
請回答下列問題:
(1)假設某溫度下,反應Ⅰ的速率(v1)大于反應Ⅱ的速率(v2),則下列反應過程能量變化示意圖正確的是_____________。
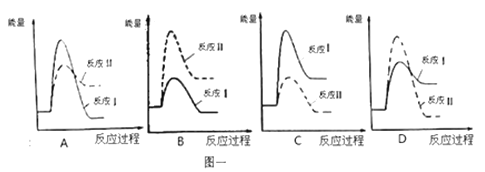
(2)通過監測反應體系中氣體濃度的變化可判斷反應Ⅰ和Ⅱ是否同時發生,理由是 ______________。
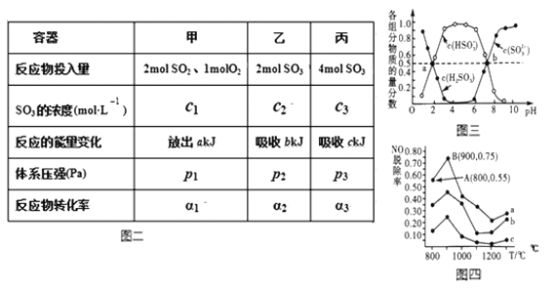
(3)在溫度、容積相同且不變的3個密閉容器中,按不同方式投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如圖二(已知2SO2(g)+O2(g)=2SO3(g) △H=196.6kJ·mol-1)
A.2c1______c3 B.a+b______196.6 C.2p2______p3 D.α1+α3______1(填>,=,<)
(4) “亞硫酸鹽法”吸收煙氣中的SO2。室溫條件下,將煙氣通入氨水溶液中,測得溶液pH與含硫組分物質的量分數的變化關系如圖三所示。
請寫出a點時n(HSO3-):n(H2SO3)=______,b點時溶液pH=7,則n(NH4+):n(HSO3-)=___。
(5)催化氧化法去除NO,一定條件下,用NH3消除NO污染,其反應原理為4NH3+6NO![]() 5N2+ 6H2O。不同溫度條件下,n(NH3):n(NO)的物質的量之比分別為4:l、3:l、1:3時,得到NO脫除率曲線如圖四所示:
5N2+ 6H2O。不同溫度條件下,n(NH3):n(NO)的物質的量之比分別為4:l、3:l、1:3時,得到NO脫除率曲線如圖四所示:
①曲線c對應NH3與NO的物質的量之比是______。
② 曲線a中NO的起始濃度為6×10-4mg/m3,從A點到B點經過0.8s,該時間段內NO的脫除速率為_____mg/(m3·s)。
(6)已知Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.5×10-9,向0.4mol/LNa2SO4的溶液中加入足量BaCO3粉末(忽略體積變化),充分攪拌,發生反應SO![]() (aq)+BaCO3 (s) BaSO4 (s)+CO
(aq)+BaCO3 (s) BaSO4 (s)+CO![]() (aq) 靜置后沉淀轉化達到平衡。此時溶液中的c(SO
(aq) 靜置后沉淀轉化達到平衡。此時溶液中的c(SO![]() )=________mol·L-1(小數點后兩位).
)=________mol·L-1(小數點后兩位).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某烴的相對分子質量為56。
(1)該烴的分子式為_________________________。
(2)若能使酸性KMnO4溶液褪色,則可能的結構簡式為__________________________。
(3)上述(2)中的混合物與足量H2反應后,所得產物共有__________種。
(4)上述(2)中的混合物若與足量HBr反應后,所得產物共有______種。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用雙線橋及單線橋表示反應3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 電子轉移情況。
雙線橋________________________________________。
單線橋________________________________________。
該反應中氧化劑是:_______。若有4molHNO3參加反應,轉移電子的物質的量為______mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)科學家發現,食用蝦類等水生甲殼類動物的同時服用維生素C容易中毒,這是因為對人體無害的+5價砷類化合物在維生素C的作用下能夠轉化為有毒的+3價的含砷化合物。通過以上信息填空:上述過程中+5價砷類物質作為______(填氧化劑或還原劑),+5價砷元素發生______反應(填氧化或還原);0.5mol+5價砷完全轉化為+3價砷,共轉移______個電子。
(2)實驗室常用以下方法制取氯氣:MnO2+4HCl(濃)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
①用雙線橋標出電子轉移方向和數目______;(在答題紙上標)
②在標準狀況下生成的氯氣為11.2L時,被氧化的HCl的質量為______;
③為保證實驗安全,常用氫氧化鈉溶液吸收多余的氯氣,寫出反應的離子方程式______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com