
某學(xué)生用0.10 mol/L標(biāo)準(zhǔn)NaOH溶液滴定某濃度的鹽酸。記錄數(shù)據(jù)如下:
| 實(shí)驗(yàn)序號(hào) | 待測液體積(mL) | 所消耗NaOH標(biāo)準(zhǔn)液的體積(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.54 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.36 |

(1)當(dāng)?shù)稳胱詈笠坏螛?biāo)準(zhǔn)液,溶液由無色變?yōu)闇\紅色,且半分鐘內(nèi)不退色
(2)0.10mol/L (3) 偏高(4) 甲 5Fe2+ + MnO4- + 8H+ = 5Fe2+ + Mn2+ + 4H2O
解析試題分析:(1)因?yàn)檫@是由已知濃度的堿滴定未知濃度的酸,酚酞指示劑在酸溶液中,是無色的,隨著堿的滴加,溶液的酸性逐漸減弱,當(dāng)?shù)渭拥阶詈笠坏螘r(shí),溶液由無色變?yōu)闇\紅色,半分鐘內(nèi)不褪色時(shí)酸堿中和恰好完成。(2)堿溶液的平均體積為V=(V1+V2+V3)÷3=" ((20.54-0.05)+(26.00-6.00)" +(21.36-1.40)) ÷3=20.00ml,利用酸堿恰好發(fā)生中和反應(yīng)時(shí)C酸??V酸=C堿?V堿,C酸="(" C堿?V堿) ÷V酸="(0.10" mol/L×20.00ml) ÷20.00ml="0.10mol/L." (3)若在滴定前堿式滴定管尖嘴部分有氣泡,滴定后消失,堿溶液的體積偏大,以此為標(biāo)準(zhǔn)計(jì)算的酸的濃度偏高。(4)若用已知準(zhǔn)確濃度的高錳酸鉀溶液滴定溶液中Fe2+的濃度,由于高錳酸鉀溶液有強(qiáng)的氧化性,容易腐蝕堿式滴定管的橡膠管,所以應(yīng)盛放在酸式滴定管甲中,發(fā)生該反應(yīng)的離子方程式為5Fe2+ + MnO4- + 8H+ = 5Fe2+ + Mn2+ + 4H2O。
考點(diǎn):考查滴定法的應(yīng)用、酸堿中和滴定終點(diǎn)的判斷、誤差分析等知識(shí)。


 閱讀快車系列答案
閱讀快車系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:填空題
已知醋酸和鹽酸是日常生活中極為常見的酸,在一定條件下,CH3COOH溶液中存在電離平衡:CH3COOH CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)常溫下,在pH=5的稀醋酸溶液中,c(CH3COO-)= (列式,不必化簡);下列方法中,可以使0.10 mol·L-1 CH3COOH的電離程度增大的是 。
a.加入少量0.10 mol·L-1的稀鹽酸
b.加熱CH3COOH溶液
c.加水稀釋至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化鈉固體
f.加入少量0.10 mol·L-1的NaOH溶液
(2)將等質(zhì)量的鋅投入等體積且pH均等于3的醋酸和鹽酸溶液中,經(jīng)過充分反應(yīng)后,發(fā)現(xiàn)只在一種溶液中有鋅粉剩余,則生成氫氣的體積:V(鹽酸) V(醋酸),反應(yīng)的最初速率為:v(鹽酸) v(醋酸)(填“>”、“<”或“=”)。
(3)常溫下,向體積為Va mL,pH為3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,則Va與Vb的關(guān)系是 。
(4)常溫下,將0.1 mol/L鹽酸和0.1 mol/L醋酸鈉溶液混合,所得溶液為中性,則混合溶液中各離子的濃度按由大到小排序?yàn)?u> 。
(5)已知:90 ℃時(shí),水的離子積常數(shù)為KW=3.8×10-13,在此溫度下,將pH=3的鹽酸和pH=11的氫氧化鈉溶液等體積混合,則混合溶液中的c(H+)= (保留三位有效數(shù)字) mol/L。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
難溶性雜鹵石(K2SO4·MgSO4·2CaSO4·2H2O)屬于“呆礦”,在水中存在如下平衡:
K2SO4·MgSO4·2CaSO4·2H2O(s) 2Ca2++2K++Mg2++4SO42—+2H2O
2Ca2++2K++Mg2++4SO42—+2H2O
為能充分利用鉀資源,用飽和Ca(OH)2溶液溶浸雜鹵石制備硫酸鉀,工藝流程如下: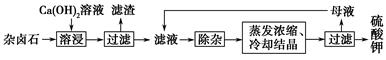
(1)濾渣主要成分有________和________以及未溶雜鹵石。
(2)用化學(xué)平衡移動(dòng)原理解釋Ca(OH)2溶液能溶解雜鹵石浸出K+的原因:_________________________________________________。
(3)“除雜”環(huán)節(jié)中,先加入________溶液,經(jīng)攪拌等操作后,過濾,再加入________溶液調(diào)濾液pH至中性。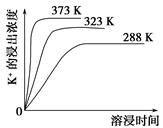
(4)不同溫度下,K+的浸出濃度與溶浸時(shí)間的關(guān)系如圖。由圖可得,隨著溫度升高,
①________________________________________________________,
②________________________________________________________。
(5)有人以可溶性碳酸鹽為溶浸劑,則溶浸過程中會(huì)發(fā)生:CaSO4(s)+CO32— CaCO3(s)+SO42—
CaCO3(s)+SO42—
已知298 K時(shí),Ksp(CaCO3)=2.80×10-9,
Ksp(CaSO4)=4.90×10-5,求此溫度下該反應(yīng)的平衡常數(shù)K(計(jì)算結(jié)果保留三位有效數(shù)字)。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
已知0.1mol/L H2SO4在水中的第一步電離是完全的,第二步電離并不完全。常溫下有0.1mol/L的以下幾種溶液的電離度(即已經(jīng)電離的分子數(shù)占原來分子總數(shù)的百分?jǐn)?shù))如下表,回答下列問題:
| ①H2SO4溶液中的HSO4– | ②NaHSO4溶液中的HSO4– | ③CH3COOH | ④HCl溶液 |
| 10% | 29% | 1.33% | 100% |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(1)25 ℃時(shí),0.1 mol·L-1NaOH溶液的pH為________;
(2)25 ℃時(shí),0.1 mol·L-1NH4Cl溶液的pH________7(填“<”、“=”或“>”),其原因是__________________(用離子方程式表示);
(3)將上述兩種溶液等體積混合后,離子濃度大小次序正確的是________(填序號(hào))。
| A.[Na+]>[Cl-]>[OH-]>[H+] |
| B.[Na+]=[Cl-]>[H+]>[OH-] |
| C.[Na+]=[Cl-]>[OH-]>[H+] |
| D.[Cl-]>[Na+]>[OH-]>[H+] |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
最近霧霾天氣肆虐我國大部分地區(qū)。其中SO2是造成空氣的污染的主要原因,利用鈉堿循環(huán)法可除去SO2。
(1)鈉堿循環(huán)法中,吸收液為Na2SO3溶液,該反應(yīng)的離子方程式是________。
(2)已知H2SO3的電離常數(shù)為K1=1.54×10-2,K2=1.024×10-7;H2CO3的電離常數(shù)為K1=4.30×10-7,K2=5.60×10-11,則下列微粒可以大量共存的是______(填序號(hào))。
A.CO32- HSO3- B. HCO3- HSO3- C. SO32- HCO3- D. H2SO3 HCO3-
(3)吸收液吸收SO2的過程中,pH隨n(SO32-):n(HSO3-)變化關(guān)系如下表:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
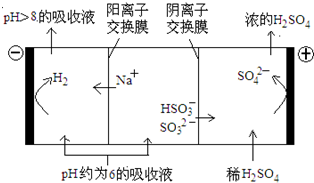
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
在室溫下,下列五種溶液:
①0.1mol/L NH4Cl
②0.1mol/L CH3COONH4
③0.1mol/L NH4HSO4
④0.1mol/L NH3·H2O和0.1mol/L NH4Cl的混合液
請根據(jù)要求填寫下列空白:
(1)溶液①呈酸性,其原因是_______________________________(用離子方程式表示)
(2)比較溶液②、③中c(NH4+)的大小關(guān)系是② ③(填“>”“=”或“<”)。
(3)在溶液④中, 離子的濃度為0.1mol/L;NH3·H2O和 離子的濃度之和為0.2 mol/L。
(4)室溫下,測得溶液②的pH=7, CH3COO-與NH4+濃度的大小關(guān)系是:
c(CH3COO-) c(NH4+)(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
請回答下列問題:
(1)若分別將pH=2的鹽酸和醋酸稀釋100倍,則稀釋后溶液的pH:鹽酸 醋酸(填“>”、“=”或“<”)。
(2)將100mL 0.1mol?L-1的CH3COOH溶液與50mL 0.2mol?L-1的NaOH溶液混合,所得溶液呈 性,原因是 (用離子方程式表示)。
(3)0.1mol·mol-1的氨水溶液中存在電離平衡NH3+H2O  NH3·H2O
NH3·H2O NH4++OH-,在此平衡體系中改變條件(見下表),請完成表中空格:
NH4++OH-,在此平衡體系中改變條件(見下表),請完成表中空格:
| | 條件的變化 | 通氨氣 | 加水 | 加NH4Cl(s) |
| ① | 電離平衡移動(dòng)的方向 | | | |
| ② | c(OH-)的變化 | | | |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
結(jié)合下表回答下列問題(均為常溫下的數(shù)據(jù)):
| 酸 | 電離常數(shù)(Ka) | 酸 | 電離常數(shù)(Ka) |
| CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
| HClO | 3×10-8 |
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com