
【題目】下圖為實驗室制取純凈、干燥的Cl2 , 并進行檢驗Cl2性質實驗的裝置。其中E瓶中放有干燥紅色布條;F中為銅網,F右端出氣管口附近放有脫脂棉。
試回答:
(1)A中所放試劑為 , B中所放試劑為 , 二者反應的化學方程式為 , 該反應中的氧化劑是;
(2)C中試劑是;D中試劑的作用是;
(3)E中現象是; F中現象是 , 其反應的化學方程式為;F管中脫脂棉的作用是
(4)H中試劑為;
(5)整套裝置中有兩處用酒精燈加熱,兩處酒精燈點燃的先后順序是(用①或②填寫)。
【答案】
(1)濃鹽酸,MnO2,MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O,MnO2
MnCl2+Cl2↑+2H2O,MnO2
(2)飽和食鹽水,吸水氯氣中的水蒸氣
(3)干燥的紅色布條不褪色,棕黃色的煙,Cu+Cl2![]() CuCl2,防止CuCl2固體小顆粒被氣體鼓入導管中,堵塞導管
CuCl2,防止CuCl2固體小顆粒被氣體鼓入導管中,堵塞導管
(4)NaOH溶液
(5)先②后①
【解析】(1)實驗室是利用二氧化錳和濃鹽酸加熱反應生成氯氣,A中是濃鹽酸,B中是二氧化錳固體,反應的化學方程式為:MnO2+4HCl(濃) ![]() MnCl2+Cl2↑+2H2O;反應中Mn元素化合價降低,得到電子,二氧化錳是氧化劑;
MnCl2+Cl2↑+2H2O;反應中Mn元素化合價降低,得到電子,二氧化錳是氧化劑;
(2)生成的氯氣中含有氯化氫和水蒸氣,可以用飽和食鹽水除去氯氣中的氯化氫,用濃硫酸除去氯氣中的水蒸氣得到干燥純凈的氯氣;
(3)E是收集氯氣并檢驗氯氣是否具有漂白性的實驗裝置,氯氣無漂白性,干燥的有色布條不褪色;F是銅加熱和氯氣反應生成氯化銅的反應,生成的氯化銅形成棕色煙,反應的化學方程式為Cu+Cl2![]() CuCl2;脫脂棉的主要作用是防止固體氯化銅小顆粒進入導氣管堵塞導管;
CuCl2;脫脂棉的主要作用是防止固體氯化銅小顆粒進入導氣管堵塞導管;
(4)氯氣有毒,不能排放到空氣中,需要用氫氧化鈉溶液吸收,氯氣和氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉和水;
(5)銅在加熱的條件下易與空氣反應,因此酒精燈需要先點燃①處生成氯氣充滿裝置②后,再點燃②處酒精燈,以防止銅和空氣中的氧氣反應。
【考點精析】利用氯氣的實驗室制法對題目進行判斷即可得到答案,需要熟知實驗室制法:MnO2+4HCl(濃)=MnCl2+Cl2↑+2H2O.


 尖子生新課堂課時作業系列答案
尖子生新課堂課時作業系列答案科目:高中化學 來源: 題型:
【題目】有人設想用SO2制取少量硫酸,其裝置如圖所示: 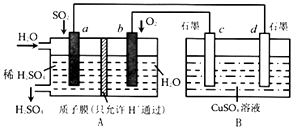
①H+移向極(填“a”或“b”),c極的電極名稱是 ,
②a極發生的電極反應式為 .
③c極發生的電極反應式為 .
④標準狀況下,A裝置吸收3.36LSO2時,B裝置中溶液最多減重g.(裝置中氣體的溶解性忽略不計)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮氧化鋁(AlON)屬原子晶體,是一種超強透明材料,可以由反應Al2O3+C+N2 ![]() 2AlON+CO合成,下列有關說法正確的是( )
2AlON+CO合成,下列有關說法正確的是( )
A.氮氧化鋁中氮的化合價是﹣3
B.反應中氧化產物和還原產物的物質的量之比是1:2
C.反應中每生成5.7gAlON同時生成1.12LCO
D.AlON和CO的化學鍵類型不同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某強氧化劑[RO(OH)2]2+離子2.4×10-3mol被亞硫酸鈉還原到較低價態,需12mL0.2mol/L的亞硫酸鈉溶液,則反應后R的化合價為( )
A.0B.+2C.+3D.+4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一包鐵粉和氧化銅混合均勻的粉末樣品4.40g,加入50mL稀硫酸恰好充分反應后,得到只含一種金屬陽離子的淺綠色溶液和1.28g固體銅.并放出H2 . 試計算:
(1)固體銅的物質的量為mol,該樣品中鐵粉和氧化銅的物質的量之比為 .
(2)硫酸的物質的量的濃度molL﹣1 , 產生H2在標準狀況下的體積L.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將CO2氣體緩緩通入到含有等物質的量的KOH,Ba(OH)2和KAlO2的混合溶液中,直至過量,生成沉淀的物質的量與所通CO2的體積關系如圖所示(假設每步反應均完全).下列關于整個反應進程中的各種描述不正確的是( ) 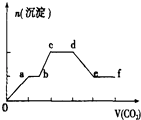
A.d~e段沉淀的減少是由碳酸鋇固體的消失所致
B.b~c段反應的離子方程式是:2A1O2﹣+3H2O+CO2=2A1(OH)3↓+CO32﹣
C.0~a段反應的化學方程式是:Ba(OH)2+CO2=BaCO3↓+H2O
D.a~b段與c~d段所發生的反應相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的認識不正確的是( )
A.油脂在空氣中完全燃燒轉化為水和二氧化碳
B.蔗糖、麥芽糖的分子式都是C12H22O11,二者互為同分異構體
C.在水溶液里,乙酸分子中的-CH3可以電離出H+
D.在濃硫酸存在下,苯與濃硝酸共熱生成硝基苯的反應屬于取代反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知熱化學方程式:SO2(g)+ ![]() O2(g)SO3(g)△H=﹣98.32kJ/mol,在容器中充入2molSO2和1molO2充分反應,最終放出的熱量為( )
O2(g)SO3(g)△H=﹣98.32kJ/mol,在容器中充入2molSO2和1molO2充分反應,最終放出的熱量為( )
A.98.32kJ
B.196.64kJ/mol
C.<196.64kJ
D.>196.64kJ
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com