
制備食用碘鹽(KIO3)原理之一為:I2+2KClO3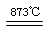 Cl2+2KIO3,下列說法正確的是
Cl2+2KIO3,下列說法正確的是
| A.向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀 |
| B.反應過程中I2置換出Cl2,由此可推斷非金屬性I>CI |
| C.KClO3和KIO3均屬于離子化合物,都只含有離子鍵 |
| D.制備KIO3的反應中氯元素被還原 |
D
解析試題分析:A、氯酸鉀在溶液中電離出的離子是K+、ClO3-,所以向KClO3溶液中滴加AgNO3溶液得不到白色AgCl沉淀,A不正確;B、反應過程中I2置換出Cl2,但該反應不是在溶液中進行的,所以不能依據該反應推斷非金屬性I>CI,事實上非金屬性是I<CI,B不正確;C、KClO3和KIO3均屬于離子化合物,都含有離子鍵,另外氯元素與氧元素、以及碘元素與氧元素之間還存在共價鍵,C不正確;D、反應中氯元素的化合價從+5價降低到0價,得到電子,被還原,所以制備KIO3的反應中氯元素被還原,D正確,答案選D。
考點:考查物質組成、非金屬性比較、化學鍵判斷以及氧化還原反應的有關應用


科目:高中化學 來源: 題型:單選題
FeS2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-的形式存在。若有l mol FeS2“溶解”,則生成H2SO4的物質的量為
| A.2mol | B.4 mol | C.6 mol | D.8 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
三氟化氮(NF3)是微電子工業中一種優良的等離子蝕刻氣體。它無色、無臭,在潮濕的空氣中能發生下列反應:3NF3+5H2O 2NO+HNO3+9HF,下列有關說法正確的是( )
2NO+HNO3+9HF,下列有關說法正確的是( )
| A.反應中NF3是氧化劑,H2O是還原劑 |
| B.反應中被氧化與被還原的原子物質的量之比為2∶1 |
| C.若反應中生成0.2 mol HNO3,則反應共轉移0.2 mol e- |
| D.NF3在潮濕的空氣中泄漏會產生白霧、紅棕色氣體等現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
將51.2 g Cu完全溶于適量濃硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,這些氣體恰好能被500 mL 2 mol/L NaOH溶液完全吸收,發生的反應為:
2NO2+2NaOH=NaNO2+NaNO3+H2O; NO+NO2+2NaOH=2NaNO2+H2O。
則生成的鹽溶液中NaNO2的物質的量為( )
| A.0.4 mol | B.0.6 mol | C.0.8 mol | D.0.2 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
Na2FeO4是一種高效多功能水處理劑,一種制備Na2FeO4的方法可用化學方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2 +O2↑。下列對此反應的說法中,不正確的是( )
+O2↑。下列對此反應的說法中,不正確的是( )
| A.方框中的物質為Na2SO4 |
| B.Na2O2既是氧化劑,又是還原劑 |
| C.Na2FeO4既是氧化產物,又是還原產物 |
| D.2 mol FeSO4發生反應時,反應中共轉移8 mol電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
LiAlH4是金屬儲氫材料又是有機合成中的常用試劑,遇水能劇烈反應釋放出氫氣,LiAlH4在125 ℃分解為LiH、H2和Al。下列敘述錯誤的是( )。
| A.LiAlH4與乙醛作用生成乙醇,LiAlH4作還原劑 |
| B.LiAlH4與D2O反應,所得氫氣的摩爾質量為4 g·mol-1 |
| C.1 mol LiAlH4在125 ℃完全分解,轉移3 mol電子 |
| D.LiAlH4與水反應生成三種物質時,化學方程式可表示為:LiAlH4+4H2O=Al(OH)3+LiOH+4H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
日常生活中的許多現象與化學反應有關,下列現象與氧化還原反應無關的是( )
| A.銅鑄塑像上出現銅綠[Cu2(OH)2CO3] |
| B.用石膏粉制作石膏雕像 |
| C.用鋁質或鐵質容器盛放濃硝酸 |
| D.酸雨的形成 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
氯酸是一種強酸,濃度超過40%時會發生分解,該反應可表示為aHClO3―→bO2↑+cCl2↑+dHClO4+eH2O,下列有關說法不正確的是 ( )。
| A.由反應可確定氧化性:HClO3>O2 |
| B.由非金屬性:Cl>S,可推知酸性:HClO3>H2SO4 |
| C.若氯酸分解所得1 mol混合氣體的質量為45 g,則反應的化學方程式可表示為3HClO3===2O2↑+Cl2↑+HClO4+H2O |
| D.若化學計量數a=8,b=3,則生成3 mol O2時該反應轉移20 mol電子 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com