
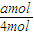 =
=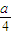 ,故答案為:
,故答案為: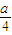 ;
;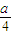 ,所以C的物質的量為
,所以C的物質的量為 ×(2mol+6mol)=2amol,故答案為:2amol;
×(2mol+6mol)=2amol,故答案為:2amol; n)mol:(8+
n)mol:(8+ n)mol=1:3,
n)mol=1:3, m,
m, m.
m.

 學練快車道口算心算速算天天練系列答案
學練快車道口算心算速算天天練系列答案科目:高中化學 來源: 題型:閱讀理解
 氮是地球上含量豐富的元素,氮及其化合物的研究在生產、生活中有著重要意義.
氮是地球上含量豐富的元素,氮及其化合物的研究在生產、生活中有著重要意義.| 1 |
| 2 |
| 3 |
| 2 |
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
| C4(NO)C6(H2O) |
| C4(NH3)C5(O2) |
| C4(NO)C6(H2O) |
| C4(NH3)C5(O2) |
| 催化劑 |
| 高溫高壓 |
| 容器 編號 |
起始時各物質的物質的量/mol | 反應達平衡時的焓變/kJ?mol-1 | ||
| N2 | H2 | NH3 | ||
| A | 1 | 3 | 0 | △H1=-23.1 |
| B | 0.9 | 2.7 | 0.2 | △H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
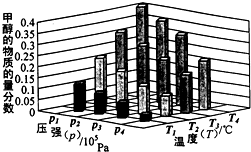 能源是制約國家發展進程的因素之一.甲醇、二甲醚等被稱為2 1世紀的綠色能源,工業上利用天然氣為主要原料與二氧化碳、水蒸氣在一定條件下制備合成氣(CO、H2),再制成甲醇、二甲醚.
能源是制約國家發展進程的因素之一.甲醇、二甲醚等被稱為2 1世紀的綠色能源,工業上利用天然氣為主要原料與二氧化碳、水蒸氣在一定條件下制備合成氣(CO、H2),再制成甲醇、二甲醚.查看答案和解析>>
科目:高中化學 來源:2011屆浙江省杭州高級中學高三高考全真模擬卷(理綜)化學試題 題型:填空題
氮是大氣中含量豐富的一種元素,氮及其化合物在生產、生活中有著重要作用,減少氮氧化物的排放是環境保護的重要內容之一。請回答下列氮及其化合物的相關問題:
(1)據報道,意大利科學家獲得了極具研究價值的N4,其分子結構與白磷分子的正四面體結構相似。已知斷裂1 mol N-N鍵吸收167 kJ熱量,生成1 mol N≡N鍵放出942 kJ熱量,請寫出N4氣體轉變為N2反應的熱化學方程式:______________________。
(2)據報道,NH3可直接用作車用燃料電池,寫出該電池的負極反應式:
__________________________________________________________________________。
(3)在T1℃時,將5 mol N2O5置于10 L固定容積的密閉容器中發生下列反應:2N2O5(g) 4NO2(g)+O2(g);△H>0。反應至5分鐘時各物質的濃度不再發生變化,測得NO2的體積分數為50%。
4NO2(g)+O2(g);△H>0。反應至5分鐘時各物質的濃度不再發生變化,測得NO2的體積分數為50%。
①上述平衡體系中O2的體積分數為__________,N2O5的物質的量為__________mol。
②用O2表示從0~5 min內該反應的平均速率υ(O2)= __________。
③將上述平衡體系的溫度降至T2℃,密閉容器內減小的物理量有__________。
A.壓強 B.密度 C.反應速率 D.N2O5的濃度
(4)在恒溫恒容的密閉容器中充入NO2,建立如下平衡:2NO2(g) N2O4(g),平衡時N2O4與NO2的物質的量之比為a,其它條件不變的情況下,分別再充入NO2和再充入N2O4,平衡后引起的變化正確的是__________。
N2O4(g),平衡時N2O4與NO2的物質的量之比為a,其它條件不變的情況下,分別再充入NO2和再充入N2O4,平衡后引起的變化正確的是__________。
A.都引起a減小 B.都引起a增大
C.充入NO2引起a減小,充入N2O4引起a增大
D.充入NO2引起a增大,充入N2O4引起a減小
查看答案和解析>>
科目:高中化學 來源:2014屆浙江省溫州市十校聯合體高三上學期期中聯考化學試卷(解析版) 題型:填空題
氮是大氣中含量豐富的一種元素,氮及其化合物在生產、生活中有著重要作用,減少氮氧化物的排放是環境保護的重要內容之一。請回答下列氮及其化合物的相關問題:
(1)據報道,意大利科學家獲得了極具研究價值的N4,其分子結構與白磷分子的正四面體結構相似。已知斷裂1 mol N-N鍵吸收167 kJ熱量,生成1 mol N≡N鍵放出942 kJ熱量,請寫出N4氣體轉變為N2反應的熱化學方程式: 。
(2)據報道,NH3可直接用作車用燃料電池,寫出該電池的負極反應式: 。
(3)在T1℃時,將5 mol N2O5置于10L固定容積的密閉容器中發生下列反應:2N2O5(g) 4NO2(g)+O2(g);△H>0。反應至5分鐘時各物質的濃度不再發生變化,測得NO2的體積分數為50%。
4NO2(g)+O2(g);△H>0。反應至5分鐘時各物質的濃度不再發生變化,測得NO2的體積分數為50%。
①求該反應的平衡常數K= (數字代入式子即可),上述平衡體系中O2的體積分數為__________。
②用O2表示從0~5 min內該反應的平均速率υ(O2)= 。
③將上述平衡體系的溫度降至T2℃,密閉容器內減小的物理量有 。
A.壓強 B.密度 C.反應速率 D.N2O5的濃度
(4)在恒溫恒容的密閉容器中充入NO2,建立如下平衡:2NO2(g) N2O4(g),平衡時N2O4與NO2的物質的量之比為a,其它條件不變的情況下,分別再充入NO2和再充入N2O4,平衡后引起的變化正確的是__________。
N2O4(g),平衡時N2O4與NO2的物質的量之比為a,其它條件不變的情況下,分別再充入NO2和再充入N2O4,平衡后引起的變化正確的是__________。
A.都引起a減小 B.都引起a增大 C.充入NO2引起a減小,充入N2O4引起a增大
D.充入NO2引起a增大,充入N2O4引起a減小
查看答案和解析>>
科目:高中化學 來源: 題型:
一定條件下將2mol SO2和2mol SO3氣體混合于一固定容積的密閉容器中,發生反應:
2SO2+O2 ![]() 2SO3,平衡時SO3為n mol,在相同溫度下,分別按下列配比在上述容
2SO3,平衡時SO3為n mol,在相同溫度下,分別按下列配比在上述容
器中放入起始物質,平衡時SO3的物質的量可能大于n的是 ( )
A.2 mol SO2 + 1 mol O2 B.4 mol SO2 + 1 mol O2
C.2 mol SO2 + 1 mol O2 + 2 SO3 D.3 mol SO2 + 1 SO3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com