
下列事實能說明影響化學反應(yīng)速率的決定性因素是反應(yīng)物本身性質(zhì)的是( )
| A.Cu能與濃硝酸反應(yīng),而不與濃鹽酸反應(yīng) |
| B.Cu與濃硝酸反應(yīng)比與稀硝酸反應(yīng)快 |
| C.N2與O2在常溫、常壓下不反應(yīng),放電時可反應(yīng) |
| D.Cu與濃硫酸反應(yīng),而不與稀硫酸反應(yīng) |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應(yīng)用題系列答案
小學生10分鐘應(yīng)用題系列答案科目:高中化學 來源: 題型:單選題
在一密閉容器中,反應(yīng) aA(g)  bB(g)+cC(g)達平衡后,保持溫度不變,將容器體積增加一倍,最終測得A的物質(zhì)的量的濃度變?yōu)樵瓉淼?0%,則
bB(g)+cC(g)達平衡后,保持溫度不變,將容器體積增加一倍,最終測得A的物質(zhì)的量的濃度變?yōu)樵瓉淼?0%,則
| A.平衡向正反應(yīng)方向移動 | B.a(chǎn)>(b+c) |
| C.物質(zhì)B的質(zhì)量分數(shù)增大 | D.以上判斷都錯誤 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
將等質(zhì)量的兩份鋅粉a、b分別加入過量的稀硫酸,同時向a中加少量的CuSO4溶液,如各圖中產(chǎn)生H2的體積V(L)與時間t(min)的關(guān)系,正確的是( )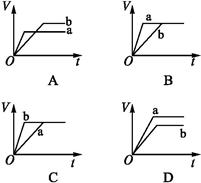
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列反應(yīng)中,在高溫下不能自發(fā)進行的是( )
A.CO(g) C(s)+O2(g) C(s)+O2(g) |
B.NH4Cl(s) NH3(g)↑+HCl(g)↑ NH3(g)↑+HCl(g)↑ |
C.(NH4)2CO3(s) NH4HCO3(s)+NH3(g) NH4HCO3(s)+NH3(g) |
D.MgCO3(s) MgO(s)+CO2(g) MgO(s)+CO2(g) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
對于化學反應(yīng)方向的確定不僅與焓變(ΔH)有關(guān),也與溫度(T)、熵變(ΔS)有關(guān),實驗證明,化學反應(yīng)的方向應(yīng)由ΔH-TΔS確定,若ΔH-TΔS<0,則自發(fā)進行,否則不能自發(fā)進行。下列說法中,正確的是( )
| A.在溫度、壓強一定的條件下,焓因素和熵因素共同決定一個化學反應(yīng)的方向 |
| B.溫度、壓強一定時,熵增加的反應(yīng)一定能自發(fā)進行 |
| C.反應(yīng)焓變是決定反應(yīng)能否自發(fā)進行的唯一因素 |
| D.固體的溶解過程只與焓變有關(guān) |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知反應(yīng):A(g)+3B(g) 2C(g)是放熱反應(yīng),達到平衡后,將氣體混合物的溫度降低,下列敘述中正確的是( )
2C(g)是放熱反應(yīng),達到平衡后,將氣體混合物的溫度降低,下列敘述中正確的是( )
| A.正反應(yīng)速率增大,逆反應(yīng)速率變小,平衡向正反應(yīng)方向移動 |
| B.正反應(yīng)速率變小,逆反應(yīng)速率增大,平衡向逆反應(yīng)方向移動 |
| C.正反應(yīng)速率和逆反應(yīng)速率都變小,平衡向正反應(yīng)方向移動 |
| D.正反應(yīng)速率和逆反應(yīng)速率都變小,平衡向逆反應(yīng)方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在密閉容器中進行如下反應(yīng):X2(g)+3Y2(g) 2Z(g),X2、Y2、Z的起始濃度分別為0.2 mol·L-1、0.6 mol·L-1、0.4 mol·L-1,當平衡時,下列數(shù)據(jù)肯定不正確的是( )
2Z(g),X2、Y2、Z的起始濃度分別為0.2 mol·L-1、0.6 mol·L-1、0.4 mol·L-1,當平衡時,下列數(shù)據(jù)肯定不正確的是( )
| A.X2為0.3 mol·L-1,Y2為0.9 mol·L-1 | B.Y2為1.0 mol·L-1 |
| C.X2為0.3 mol·L-1,Z為0.2 mol·L-1 | D.Z為1.0 mol·L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
反應(yīng)4A(s)+3B(g) 2C(g)+D(g),經(jīng)2 min B的濃度減少0.6 mol·L-1。對此反應(yīng)速率的正確表示是( )
2C(g)+D(g),經(jīng)2 min B的濃度減少0.6 mol·L-1。對此反應(yīng)速率的正確表示是( )
A.用A表示的反應(yīng)速率是0.8 mol·L-1·s-1
B.分別用B、C、D表示反應(yīng)的速率,其比值是3∶2∶1
C.在2 min末時的反應(yīng)速率,用反應(yīng)物B來表示是0.3 mol·L-1·min-1
D.在這2 min內(nèi)用B和C表示的反應(yīng)速率的值都是相同的
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
某恒溫容器用固定隔板隔成甲、乙兩容器,如圖所示,在甲、乙兩容器中都充入1 mol A和2 mol B,反應(yīng)3A(g)+B(g) xC(g)達到平衡后,甲、乙兩容器中A物質(zhì)的濃度比為5:3,甲、乙兩容器中C的體積分數(shù)大小為 ( )
xC(g)達到平衡后,甲、乙兩容器中A物質(zhì)的濃度比為5:3,甲、乙兩容器中C的體積分數(shù)大小為 ( )
| A.甲>乙 | B.甲<乙 | C.甲=乙 | D.無法確定 |
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com