
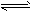 2SO3(g) △H= -196.6 KJ·mol-1)
2SO3(g) △H= -196.6 KJ·mol-1) 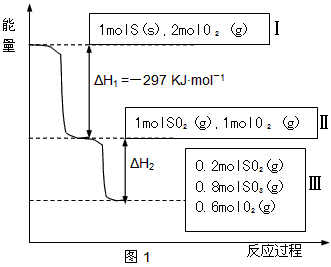
科目:高中化學 來源: 題型:閱讀理解
| 通電 |
| 加熱 |
查看答案和解析>>
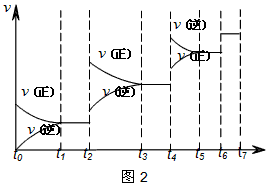
科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
| ||
| 太陽光 |
| ||
| 溫度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常數 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
查看答案和解析>>
科目:高中化學 來源:模擬題 題型:填空題
 H2+I2
H2+I2  CH3OH(g) 分析該反應并回答下列問題:
CH3OH(g) 分析該反應并回答下列問題: 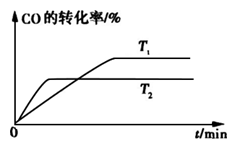

查看答案和解析>>
科目:高中化學 來源:2012-2013學年寧夏銀川一中高三(上)第三次月考化學試卷(解析版) 題型:解答題
 H2+I2Ⅲ.2H2SO4=2SO2+O2+2H2O
H2+I2Ⅲ.2H2SO4=2SO2+O2+2H2O CH3OH(g)分析該反應并回答下列問題:
CH3OH(g)分析該反應并回答下列問題: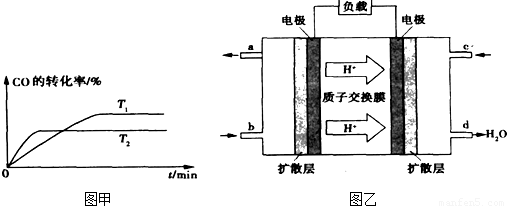
查看答案和解析>>
科目:高中化學 來源:模擬題 題型:填空題
 CH3OH(g)+H2O(g) △H<0 在一恒溫恒容密閉容器中充入1 mol CO2和3 mol H2,進行上述反應。測得CO2和CH3OH(g)的濃度隨時間變化如下圖所示。
CH3OH(g)+H2O(g) △H<0 在一恒溫恒容密閉容器中充入1 mol CO2和3 mol H2,進行上述反應。測得CO2和CH3OH(g)的濃度隨時間變化如下圖所示。 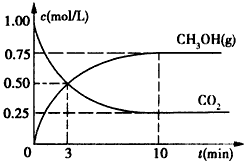
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com