
【題目】向如圖所示的裝置中緩慢地通入適量Cl2后,有色布條褪色。則X中所加物質可能是

A. 飽和食鹽水
B. 濃硫酸
C. NaOH溶液
D. FeCl2 溶液
 華東師大版一課一練系列答案
華東師大版一課一練系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化學 來源: 題型:
【題目】A 是由兩種元素組成的化合物,質量比為 7:8,在真空中加熱分解,生成 B、C。E 是常見的液體,C 和E 高溫下能發生反應。F 為日常生活中常見的化合物,E、F 之間的反應常用于工業生產,I 為黃綠色氣體單質。

(1)寫出 A 的化學式:____
(2)寫出 K 的電子式:______
(3)寫出 C 和 E 高溫下能發生反應的方程式:______
(4)寫出 D 和 L 發生反應的離子方程式:_______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】回答下列問題:
(1)將等體積等物質的量濃度的醋酸和氫氧化鈉溶液混合后,溶液呈________(填“酸性”、“中性”或“堿性”,下同),溶液中c(Na+)______c(CH3COO-)(填“>”、“=”或“<”,下同)。
(2)pH=3的醋酸和pH=11的氫氧化鈉溶液等體積混合后溶液呈________性,溶液中c(Na+)________c(CH3COO-)
(3)常溫下將0.2 mol·L-1 HCl溶液與0.2 mol·L-1 MOH溶液等體積混合,測得混合溶液的pH=6,則混合溶液中由水電離出的c(H+)________0.2 mol·L-1 HCl溶液中由水電離出的c(H+)。(填“>”、“<”或“=”,下同)
(4)常溫下若將0.2 mol·L-1MOH溶液與0.1 mol·L-1 HCl溶液等體積混合,測得混合溶液的pH<7,則說明在相同條件下MOH的電離程度________MCl的水解程度。
(5)常溫下若將pH=3的HR溶液與pH=11的NaOH溶液等體積混合,測得混合溶液的pH≠7,則混合溶液的pH________。(填“>7”、“<7”或“無法確定”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解飽和食鹽水是一項重要的化學工業,請完成下列計算:
(1)當電解產生0.2molNaOH時,能收集到標準狀況下的H2____L。
(2)已知室溫時飽和食鹽水的溶質質量分數為0.265,取200g飽和食鹽水進行電解,當NaCl反應了一半時停止電解,
①求出所得混合溶液中NaCl的質量。_____
②求出所得混合溶液中NaOH的質量分數。____(寫出計算過程,保留3位小數)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖,將潮濕的![]() 通過甲裝置后再通過放有干燥紅色布條的乙裝置,紅色布條不褪色。則甲裝置中所盛試劑不可能是
通過甲裝置后再通過放有干燥紅色布條的乙裝置,紅色布條不褪色。則甲裝置中所盛試劑不可能是

A.飽和食鹽水B.濃硫酸C.KI溶液D.NaOH溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上合成乳酸(![]() )的一種途徑如下:
)的一種途徑如下:
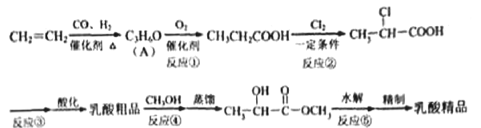
完成下列填空:
(1) 乳酸中的官能團名稱是___________ 。A 的結構簡式是___________。
(2)反應②的反應類型是___________。反應③的條件是___________。
(3)反應④的化學方程式為____________________________________________。
(4)聚乳酸是一種常用的可降解塑料,由乳酸聚合得到,其結構如下:

聚乳酸降解時,會產生自催化效應(降解的速度會越來越快) ,請解釋原因__________。
(5)設計一條由丙烯制備丙酸的合成路線 _____________________ 。
(合成路線常用的表示方式為:A ![]() B ... ...
B ... ... ![]() 目標產物)
目標產物)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 是一種常見的強氧化劑,主要用于防腐、化工、制藥等。現以某種軟錳礦
是一種常見的強氧化劑,主要用于防腐、化工、制藥等。現以某種軟錳礦![]() 主要成分
主要成分![]() ,還有
,還有![]() 、
、![]() 、
、![]() 等
等![]() 作脫硫劑,通過如下簡化流程既脫除燃煤尾氣中的
作脫硫劑,通過如下簡化流程既脫除燃煤尾氣中的![]() ,又制得
,又制得![]() 反應條件已經省略
反應條件已經省略![]() 。
。
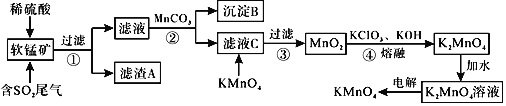
已知:![]() ,
,![]() 回答下列問題:
回答下列問題:
![]() 濾渣A的成分是
濾渣A的成分是![]() 寫化學式
寫化學式![]() ______。
______。
![]() 析出沉淀B時,首先析出的物質是
析出沉淀B時,首先析出的物質是![]() 寫化學式
寫化學式![]() ______。
______。
![]() 步驟2中加入
步驟2中加入![]() 的作用為______。
的作用為______。
![]() 濾液C中加入
濾液C中加入![]() 時發生反應的離子方程式是______。
時發生反應的離子方程式是______。
![]() 完成步驟4中反應的化學方程式______
完成步驟4中反應的化學方程式______![]() ______
______![]() ______
______![]() ______
______
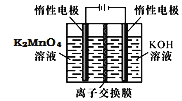
![]() 電解制備
電解制備![]() 的裝置如圖所示。電解液中最好選擇______離子交換膜
的裝置如圖所示。電解液中最好選擇______離子交換膜![]() 填“陽”或“陰”
填“陽”或“陰”![]() 。電解時,陽極的電極反應式為______。
。電解時,陽極的電極反應式為______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知在25 ℃、101 kPa下,1 g C8H18(辛烷)燃燒生成二氧化碳和液態水放出48.40 kJ熱量,表示上述反應的熱化學方程式正確的是( )
A. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=-48.40 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=-48.40 kJ·mol-1
B. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=-5 518 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=-5 518 kJ·mol-1
C. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=+5 518 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=+5 518 kJ·mol-1
D. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=+48.40 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=+48.40 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學擬用煤干餾的產物W為基本原料合成一系列化工產品,其流程如下(部分產物和條件省略):

己知部分信息如下:
①1mol芳香烴W含50mol電子;
②![]() ;
;
③![]() (苯胺,易被氧化)
(苯胺,易被氧化)
④K的分子式為C7H6O2,其核磁共振氫譜上有4個峰。
請回答下列問題:
(1)X的名稱為_________,Y中所含官能團的名稱為_________ 。
(2)反應⑦的條件為_________,②的反應類型________。
(3)反應⑤的化學方程式為_________。
(4)Z的結構簡式為_________ 。
(5)K的同分異構體M既能發生水解反應,又能發生銀鏡反應,M在氫氧化鈉溶液中發生水解反應的化學方程式為__________。
(6) 有多種同分異構體,寫出符合以下3個條件的同分異構體的結構簡式_________。
有多種同分異構體,寫出符合以下3個條件的同分異構體的結構簡式_________。
①能發生銀鏡反應但不能水解。
②每摩爾同分異構體最多消耗2molNaOH。
③苯環上一氯代物只有兩種。
(7)請以流程圖的形式寫出由T制備 的過程(無機試劑任選):(仿照
的過程(無機試劑任選):(仿照 )_____________________
)_____________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com