
【題目】鈦是一種性能非常優越的金屬,它化學性質穩定,耐腐蝕、鈦及鈦合金主要用于飛機、火箭、導彈、人造衛星和宇宙飛船等領域,某實驗室模擬硫酸法生產二氧化鈦,實驗流程如下:
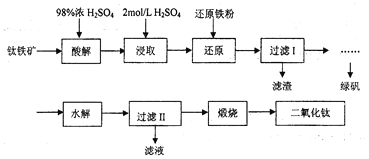
(1)酸解過程中發生的主要反應如下:FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O 請補充生成TiOSO4的化學方程式________________________________________;
(2)若取5g鈦鐵礦(主要成分是FeTiO3,含少量Fe2O3)于蒸發皿,加適量98%濃硫酸(密度1.84g/cm3)加熱,請選擇最接近的濃硫酸的用量_____________(填序號)。
A.2mL B.6mL C.25mL D.100mL
(3)在酸解后的浸取過程中,為提高浸出率可采用的方法有_____________。(任答一點)
(4)加“還原鐵粉”的目的_____________。
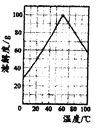
(5)請根據FeSO4溶解度曲線,補充由過慮I中濾液獲得副產品綠礬(FeSO4·7H2O)的具體操作:取過濾I所得的濾液_______________________________________________________________。
(6)“水解”過程的操作步驟:將濾液加熱至90℃,加6~7倍體積的溺水,保持沸騰60min,減壓過濾,用2mol/LH2SO4溶液洗滌沉淀,請思考,“將濾液加熱至90℃”作用是_____________________________。沉淀用2mol/LH2SO4溶液洗滌而不是用水洗滌的原因_____________________________。
【答案】
(1)FeTiO3+2H2SO4=TiOSO4+FeSO4+2H2O
(2)B
(3)粉碎礦石、適量處長浸取時間等
(4)將溶液中的Fe3+還原成Fe2+
(5)加熱濃縮到60℃飽和溶液,冷卻至0℃結晶、過濾,少量冰水洗滌、低溫干燥
(6)促進TiOSO4和Ti2(SO4)3的水解,防止Fe2+水解而造成產物不純
【解析】
試題分析:(1)鈦鐵礦主要成分與濃硫酸反應的主要產物是TiOSO4和FeSO4,根據反應物和生成物書寫方程式為FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O;
(2)5gFeTiO3的物質的量為![]() ,98%濃硫酸物質的量濃度 為18.4mol/L,根據反應FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O,可計算出消耗濃硫酸的體積約為5.4mL,根據FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O,可計算出消耗濃硫酸的體積約為3.5mL,則最接近的濃硫酸的用量為6mL,答案為B。
,98%濃硫酸物質的量濃度 為18.4mol/L,根據反應FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O,可計算出消耗濃硫酸的體積約為5.4mL,根據FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O,可計算出消耗濃硫酸的體積約為3.5mL,則最接近的濃硫酸的用量為6mL,答案為B。
(3)為提高“固體熔塊”水浸取時的浸出率,除了采用循環浸取、延長時間外,還可以采用升高溫度、增大反應物接觸面積、攪拌等方法,即采用將熔塊粉碎(或連續攪拌、適當升高溫度等)方法;
(4)根據2Fe3++Fe=3Fe2+可知,加“還原鐵粉”的目的是將溶液里的Fe3+還原為Fe2+;
(5)請根據FeSO4溶解度曲線,從過慮I中濾液獲得副產品綠礬(FeSO4·7H2O)的具體操作為加熱濃縮到60℃飽和溶液,冷卻至0℃結晶、過濾,少量冰水洗滌、低溫干燥;
(6)水解是吸熱過程,將濾液加熱至90℃作用是促進TiOSO4和Ti2(SO4)3的水解;沉淀用2mol/LH2SO4溶液洗滌而不是用水洗滌的原因防止Fe2+水解而造成產物不純。


 新課標階梯閱讀訓練系列答案
新課標階梯閱讀訓練系列答案科目:高中化學 來源: 題型:
【題目】2015年10月5日,我國女藥學家屠喲喲發現青蒿素(分子式為C15H22O5)治療瘧疾。而榮獲2015年諾貝爾生理學醫學獎。青蒿素的一種化學合成路線部分工藝流程(→……→表示省略了許多步驟)如下:
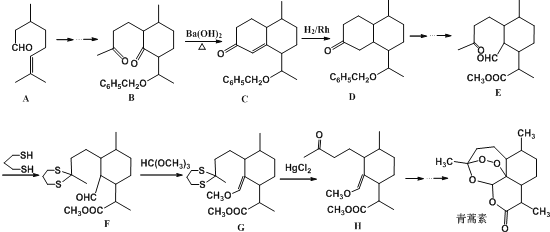
(1)1mol青蒿素完全燃燒消耗O2的物質的量為___________。
(2) A中含氧官能團的名稱___________,該物質核磁共振氫譜中一共有___________個吸收峰,C→D的反應類型___________,B→C實際上是分兩步反應進行的,先進行加成反應,再進行___________反應。
(3)寫出丙酮![]() 與
與![]() 一定條件下反應的化學方程式___________;合成路線中設計由E→F與G→H的目的是___________;
一定條件下反應的化學方程式___________;合成路線中設計由E→F與G→H的目的是___________;
(4)任寫一種同時滿足以下條件的青蒿素的同分異構體的結構簡式___________;
①能與FeC13溶液發生顯色反應
②能與NaHCO3溶液反應
③lmol該物質與足量NaOH反應消耗4mo1NaOH
④該物質核磁共振氫譜中有6組吸收峰.且峰面積之比為1:1:2:2:4:12
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(一)有機化合物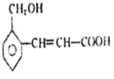 可能發生的化學反應有
可能發生的化學反應有
①加成 ②氧化 ③燃燒 ④加聚 ⑤取代
A.①②③ B.①②③④⑤ C.①②③④ D.①③④
(二)已知:A是來自石油的重要有機化工原料,E是具有果香味的有機物,F是一種高聚物,可制成食品包裝材料。
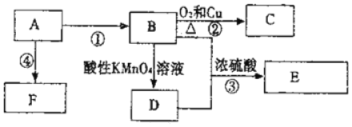
(1)A的結構簡式為 。
(2)D分子中的官能團是 。
(3)寫出下列反應的化學方程式。
② 。
④ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學課外興趣小組學生在實驗室里制取的乙烯中長混有少量的二氧化硫,老師啟發他們并由他們自己設計了下列實驗圖以確認上述混合氣體中有C2H4和SO2。回答下列問題
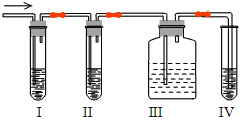
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ裝置可盛放的試劑是I ;Ⅱ ;Ⅲ ;Ⅳ 。依次填為( )
①品紅溶液 ②NaOH溶液 ③濃硫酸 ④酸性KMnO4溶液
A.④②①③ B.①②①③ C.①②①④ D.④②①④
(2)能說明SO2氣體存在的現象是____________。
(3)使用裝置Ⅲ的目的是____________。
(4)確定含有乙烯的現象是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ如圖所示:已知甲、乙、丙常溫下都為氣體。
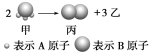
(1)乙氣體的分子式 。(用A、B表示,A、B可以選擇性使用)
(2)若測得生成物的混合氣體對氫氣的相對密度為d,則甲的摩爾質量為 。(用d表示)
(3)標準狀況下,11.2L甲氣體溶于500mL水中,所得溶液的密度為ρg/cm3,則所得溶液中甲的物質的量濃度為 (用d、ρ表示)(甲的摩爾質量用(2)中的數據)。
Ⅱ完成下列離子方程式。
(1)貝殼溶于醋酸溶液: 。
(2)向氫氧化鋇溶液中加入少量小蘇打溶液: 。
(3)碳酸氫銨和足量濃燒堿溶液混合: 。
(4)向次氯酸鈉溶液中通足量SO2氣體: 。
(5)向溴化亞鐵溶液中通入足量氯氣: 。
(6)向偏鋁酸鈉溶液中通入足量CO2氣體: 。
(7)向硫酸亞鐵溶液中加入酸性高錳酸鉀溶液: 。
(8)金屬鋅和硫酸、三氧化二砷反應生成砷化氫: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下面列出了幾組物質,請將物質的合適組號填寫在空格上。
同素異形體 , 同分異構體 。
①金剛石與“足球烯”( C60 ); ② D與T ; ③ 16O、17O和18O ;④ 氧氣(O2)與臭氧(O3); ⑤ CH4和CH3CH2CH3 ; ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑦![]() 和
和![]() ; ⑧尿素[CO(NH2)2]和 氰酸銨(NH4CNO)
; ⑧尿素[CO(NH2)2]和 氰酸銨(NH4CNO)
(2)H2O2、KCl、Na2SO4、Na2O2、NH3、O2中只含離子鍵的是 ,既有極性鍵又有非極性鍵的是 。既含離子鍵又含非極性鍵的物質的電子式是 ,請用電子式表示只含極性鍵的物質的形成過程: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種三室微生物燃料電池污水凈化系統原理如右圖所示。圖中有機廢水中有機物可用C6H10O5表示。下列有關說法正確的是
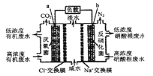
A.b電極為該電池的負極
B.b電極附近溶液的pH減小
C.a電極反應式:C6H10O5-24e-+7H2O═6CO2↑+24H+
D.中間室:Na+移向左室,Cl-移向右室
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NO2、CO、CO2是對環境影響較大的氣體,對它們的合理控制、利用是優化我們生存環境的有效途徑。
(1)如圖所示,利用電化學原理將NO2 轉化為重要化工原料C。
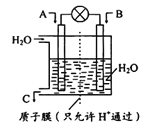
若A為NO2,B為O2,則負極的電極反應式為______________________________;
(2)有一種用CO2生產甲醇燃料的方法:
CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
已知:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-a kJ·mol-1;
CH3OH(g)+H2O(g) △H=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(g) △H=-b kJ·mol-1;
H2O(g)=H2O(l) △H=-c kJ·mol-1;
CH3OH(g)=CH3OH(l) △H=-d kJ·mol-1,
則表示CH3OH(l)燃燒熱的熱化學方程式為:_________________________________;
(3)光氣 (COCl2)是一種重要的化工原料,用于農藥、醫藥、聚酯類材料的生產,工業上通過Cl2(g)+CO(g) ![]() COCl2(g)制備。左圖為此反應的反應速率隨溫度變化的曲線,右圖為某次模擬實驗研究過程中容器內各物質的濃度隨時間變化的曲線。回答下列問題:
COCl2(g)制備。左圖為此反應的反應速率隨溫度變化的曲線,右圖為某次模擬實驗研究過程中容器內各物質的濃度隨時間變化的曲線。回答下列問題:
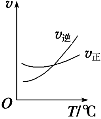
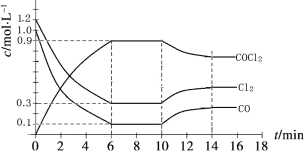
①0~6 min內,反應的平均速率v(Cl2)= ;
②若保持溫度不變,在第7min 向體系中加入這三種物質各2mol,則平衡向____________________
移動(填“向正反應方向”、“向逆反應方向”或“不”);
③若將初始投料濃度變為c(Cl2)=0.7mol/L、c(CO)=0.5mol/L、c(COCl2)_________ mol/L,保持反應溫度不變,則最終達到化學平衡時,Cl2的體積分數與上述第6min時Cl2的體積分數相同;
④隨溫度升高,該反應平衡常數變化的趨勢是__________;(填“增大”、“減小”或“不變”)
⑤比較第8min反應溫度T(8)與第15min反應溫度T(15)的高低:T(8)_______T(15)(填“<”、“>”或“=”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】印尼火山噴發不僅帶來壯觀的美景,還給附近的居民帶來物質財富,有許多居民冒著生命危險在底部的火山口收集純硫磺塊來賺取豐厚收入。硫磺可用于生產化工原料硫酸。某工廠用下圖所示的工藝流程生產硫酸:
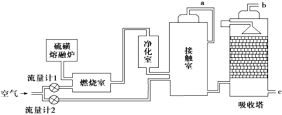
請回答下列問題:
(1)為充分利用反應放出的熱量,接觸室中應安裝______________(填設備名稱)。吸收塔中填充有許多瓷管,其作用是_____________________________________________。
(2)為使硫磺充分燃燒,經流量計1通入燃燒室的氧氣過量50%,為提高SO2轉化率,經流量計2的氧氣量為接觸室中二氧化硫完全氧化時理論需氧量的2.5倍,則生產過程中流經流量計1和流量計2的空氣體積比應為________。假設接觸室中SO2的轉化率為95%,b管排出的尾氣中二氧化硫的體積分數為__________(空氣中氧氣的體積分數按0.2計),該尾氣的處理方法是________。
(3)與以硫鐵礦為原料的生產工藝相比,該工藝的特點是________(可多選)。
A.耗氧量減少 B.二氧化硫的轉化率提高
C.產生的廢渣減少 D.不需要使用催化劑
(4)硫酸的用途非常廣,可應用于下列哪些方面__________________________。
A.橡膠的硫化 B.表面活性劑“烷基苯磺酸鈉”的合成
C.鉛蓄電池的生產 D.過磷酸鈣的制備
(5)礦物燃料的燃燒是產生大氣中SO2的主要原因之一。在燃煤中加入適量的石灰石,可有效減少煤燃燒時SO2的排放,請寫出此脫硫過程中反應的化學方程式_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com