
濃度與反應速率的關系
c(H2)/mol·L-1 | c(Cl2)/mol·L-1 | v/mol·L-1·s-1 |
1.0 | 1.0 | 1.0k |
2.0 | 1.0 | 2.0k |
2.0 | 4.0 | 4.0k |
由此可以推出,m、n的值正確的是( )?
A.m=1,n=1? B.m=![]() ,n=
,n=![]()
C.m=![]() ,n=1 D.m=1,n=
,n=1 D.m=1,n=![]()
解析:本題可以根據(jù)題中所給信息:v=kcm(H2)·cn(Cl2),選擇表中某一反應物濃度相同時的速率關系,利用數(shù)學知識進行推導計算。若選擇c(Cl2)=1.0 mol·L-1的兩種情況,則有:1.0n=![]() ,則m=1;若選擇c(H2)=2.0 mol·L-1的兩種情況,則有:
,則m=1;若選擇c(H2)=2.0 mol·L-1的兩種情況,則有:![]() ,則n=
,則n=![]() 。另外,本題也可以用代放法求解,即把表中所列c(H2)、c(Cl2)的數(shù)值與各個選項m、n的數(shù)值代入表達式v=kcm(H2)·cn(Cl2)中,若所得v值與表中的v值數(shù)據(jù)相同,則可確定為正確的選項。例如,當m=1,n=
。另外,本題也可以用代放法求解,即把表中所列c(H2)、c(Cl2)的數(shù)值與各個選項m、n的數(shù)值代入表達式v=kcm(H2)·cn(Cl2)中,若所得v值與表中的v值數(shù)據(jù)相同,則可確定為正確的選項。例如,當m=1,n=![]() 時,代入表中各個濃度數(shù)據(jù):v=k(1.0)1·(1.0)
時,代入表中各個濃度數(shù)據(jù):v=k(1.0)1·(1.0)![]() =1.0k;v=k(2.0)1·(1.0)
=1.0k;v=k(2.0)1·(1.0) ![]() =2.0k;v=k(2.0)1·(4.0)
=2.0k;v=k(2.0)1·(4.0) ![]() =4.0k。計算的v值符合已知數(shù)值,所以應該選D。?
=4.0k。計算的v值符合已知數(shù)值,所以應該選D。?
答案:D?


 培優(yōu)三好生系列答案
培優(yōu)三好生系列答案 優(yōu)化作業(yè)上海科技文獻出版社系列答案
優(yōu)化作業(yè)上海科技文獻出版社系列答案科目:高中化學 來源: 題型:閱讀理解
| ||
| ||

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 3 |
| 2 |
| 1 |
| 3 |
| 2 |
| 3 |
| 容器 | 反應物投入的量 | 反應物的轉化率 | CH3OH的濃度 | 能量變化 (Q1,Q2,Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | a1 | c1 | 放出Q1kJ熱量 |
| 乙 | 1mol CH3OH | a2 | c2 | 吸收Q2kJ熱量 |
| 丙 | 2mol CO和4mol H2 | a3 | c3 | 放出Q3kJ熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:
工業(yè)上用CO生產(chǎn)燃料甲醇。一定條件下發(fā)生反應:
CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
(1)該反應的平衡常數(shù)表達式為:K=
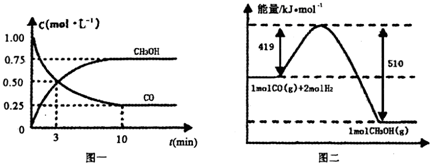
(2)圖1是反應時CO和CH3OH(g)的濃度隨時間的變化情況。從反應開始到平衡,用CO濃度變化表示的平均反應速率v(CO)= 。
(3)適宜的催化劑能 (選填序號)。
a.改變反應的熱效應 b.降低生產(chǎn)能耗 c.加快反應速率
d.提高反應物的轉化率
(4)在2 L密閉容器中發(fā)生反應CO(g)+2H2(g) ![]() CH3OH(g)若T℃時,加入2mol CH3OH,反應達平衡后,生成CO 1 mol,此時向容器中同時加入2 mol的CH3OH和4mol的H2混合氣體(保持溫度不變),則平衡將 (填“向正反應方向”、“向逆反應方向”或“不”)移動,達到新平衡后平衡常數(shù)K的值為
CH3OH(g)若T℃時,加入2mol CH3OH,反應達平衡后,生成CO 1 mol,此時向容器中同時加入2 mol的CH3OH和4mol的H2混合氣體(保持溫度不變),則平衡將 (填“向正反應方向”、“向逆反應方向”或“不”)移動,達到新平衡后平衡常數(shù)K的值為
(5)恒容條件下,下列措施中能使n (CH3OH)/n(CO)增大的有 (選填序號)。
a. 升高溫度 b. 使用催化劑 c.再充入2mol H2 d.再充入1mol CO
(6)甲醇可與氧氣構成燃料電池,該電池用多孔的惰性電極浸入濃氫氧化鉀溶液,寫出該電池的負極反應式___________________
查看答案和解析>>
科目:高中化學 來源:2011-2012學年河北省石家莊市高三補充題、壓軸題化學試卷(解析版) 題型:填空題
.(13分)我國是個鋼鐵大國,鋼鐵產(chǎn)量為世界第一,高爐煉鐵是最為普遍的煉鐵方法.
I.已知:2CO(g)+ O2(g)=2CO2(g),ΔH=-566 kJ·mol-1
2Fe(s)+
 O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
O2(g)=Fe2O3(s),ΔH=-825.5 kJ·mol-1
反應:Fe2O3(s)+
3CO(g) 2Fe(s)+ 3CO2(g),ΔH=______ kJ·mol-1.
2Fe(s)+ 3CO2(g),ΔH=______ kJ·mol-1.
Ⅱ.反應 1/3Fe2O3(s)+
CO(g) 2/3Fe(s)+ CO2(g)在1000℃的平衡常數(shù)等于4.在一個容積為10L的密閉容器中,1000℃時加入Fe、Fe2O3、CO、CO2各1.0mol,反應經(jīng)過l0min后達到平衡.
2/3Fe(s)+ CO2(g)在1000℃的平衡常數(shù)等于4.在一個容積為10L的密閉容器中,1000℃時加入Fe、Fe2O3、CO、CO2各1.0mol,反應經(jīng)過l0min后達到平衡.
(1)CO的平衡轉化率=____________.
(2)欲提高CO的平衡轉化率,促進Fe2O3的轉化,可采取的措施是________.
a.提高反應溫度 b.增大反應體系的壓強
c.選取合適的催化劑 d.及時吸收或移出部分CO2
e.粉碎礦石,使其與平衡混合氣體充分接觸
Ⅲ.高爐煉鐵產(chǎn)生的廢氣中的CO可進行回收,使其在一定條件下和H2反應制備甲醇:
CO(g)+
2H2(g) CH3OH(g).請根據(jù)圖示回答下列問題:
CH3OH(g).請根據(jù)圖示回答下列問題:

(1)從反應開始到平衡,用H2濃度變化表示平均反應速率v(H2)=________.
(2)若在溫度和容器相同的三個密閉容器中,按不同方式投入反應物,測得反應達到平衡吋的有關數(shù)據(jù)如下表:
|
容器 |
反應物投入的量 |
反應物的 轉化率 |
CH3OH的濃度 |
能量變化 (Q1、Q2、Q3均大于0) |
|
甲 |
1mol CO和2mol H2 |
α1 |
c1 |
放出Q1 kJ熱量 |
|
乙 |
1mol CH3OH |
α2 |
c2 |
吸收Q2 kJ熱量 |
|
丙 |
2mol CO和4mol H2 |
α3 |
c3 |
放出Q3 kJ熱量 |
則下列關系正確的是________.
A c1=c2 B.2Q1=Q3 C. 2α1=α2 D. α1+α2=1
E. 該反應若生成1mol CH3OH,則放出(Q1+Q2)kJ熱量
(3)若在一體積可變的密閉容器中充入l mol CO、2mol H2和1mol CH3OH,達到平衡吋測得混合氣體的密度是同溫同壓下起始的1.6倍,則該反應向________(填“正”、“逆”)反應方向移動.
(4)甲醇可與氧氣構成燃料電池,該電池用多孔的惰性電極浸入濃氫氧化鉀溶液,寫出該電池的負極反應式___ ____。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年江西省六校高三聯(lián)考(理綜)化學部分 題型:填空題
工業(yè)上用CO生產(chǎn)燃料甲醇。一定條件下發(fā)生反應:
CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。

(1)該反應的平衡常數(shù)表達式為:K=
(2)圖1是反應時CO和CH3OH(g)的濃度隨時間的變化情況。從反應開始到平衡,用CO濃度變化表示的平均反應速率v(CO)= 。
(3)適宜的催化劑能 (選填序號)。
a.改變反應的熱效應 b.降低生產(chǎn)能耗 c.加快反應速率
d.提高反應物的轉化率
(4)在2 L密閉容器中發(fā)生反應CO(g)+2H2(g)  CH3OH(g)
若T℃時,加入2mol CH3OH,反應達平衡后,生成CO 1 mol,此時向容器中同時加入2 mol的CH3OH和4mol的H2混合氣體(保持溫度不變),則平衡將
(填“向正反應方向”、“向逆反應方向”或“不”)移動,達到新平衡后平衡常數(shù)K的值為
CH3OH(g)
若T℃時,加入2mol CH3OH,反應達平衡后,生成CO 1 mol,此時向容器中同時加入2 mol的CH3OH和4mol的H2混合氣體(保持溫度不變),則平衡將
(填“向正反應方向”、“向逆反應方向”或“不”)移動,達到新平衡后平衡常數(shù)K的值為
(5)恒容條件下,下列措施中能使n (CH3OH)/n (CO)增大的有 (選填序號)。
a. 升高溫度 b. 使用催化劑 c.再充入2mol H2 d.再充入1mol CO
(6)甲醇可與氧氣構成燃料電池,該電池用多孔的惰性電極浸入濃氫氧化鉀溶液,寫出該電池的負極反應式___________________
查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com