
【題目】用以下三種途徑來制取等質量的硝酸銅。
①銅與稀硝酸反應;②銅與濃硝酸反應;③銅先與氧氣反應生成氧化銅,氧化銅再與硝酸反應。以下敘述不正確的是
A. 三種途徑所消耗銅的質量相等
B. 三種途徑所消耗硝酸的物質的量是①>②>③
C. 途徑③的制備方法最符合“綠色化學“理念
D. 途徑①中還原劑與氧化劑的物質的量之比是3: 8
【答案】BD
【解析】制取硝酸銅的有關反應①銅與稀硝酸反應:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;②銅與濃硝酸反應:Cu+4HNO3(濃)=Cu(NO3)2+2NO2↑+2H2O;③銅先與氧氣反應生成氧化銅,氧化銅再跟硝酸反應:2Cu+O2![]() 2CuO,CuO+2HNO3= Cu(NO3)2+H2O;A.銅元素都生成了硝酸銅,所以制取等量的硝酸銅消耗銅的質量相等,選項A正確;B.根據上述的反應途徑結合反應式可知三種途徑所消耗硝酸的物質的量是②>①>③,選項B錯誤;C.途徑③的制備方法中原子利用率最高,且沒有污染環境的氣體產生,所以最符合“綠色化學”理念,選項C正確;D.途徑①中被氧化的銅與被還原的硝酸的物質的量之比是3:2,選項D不正確,答案選BD。
2CuO,CuO+2HNO3= Cu(NO3)2+H2O;A.銅元素都生成了硝酸銅,所以制取等量的硝酸銅消耗銅的質量相等,選項A正確;B.根據上述的反應途徑結合反應式可知三種途徑所消耗硝酸的物質的量是②>①>③,選項B錯誤;C.途徑③的制備方法中原子利用率最高,且沒有污染環境的氣體產生,所以最符合“綠色化學”理念,選項C正確;D.途徑①中被氧化的銅與被還原的硝酸的物質的量之比是3:2,選項D不正確,答案選BD。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】白磷與氧氣可發生如下反應:P4+5O2═P4O10 . 已知斷裂下列化學鍵需要吸收的能量分別為:E(P﹣P)=a kJmol﹣1、E(P﹣O)=b kJmol﹣1、E(P=O)=c kJmol﹣1、E(O=O)=d kJmol﹣1 . 根據圖示的分子結構和有關數據估算該反應的△H,其中正確的是( ) 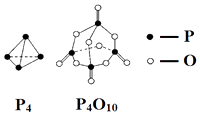
A.﹣(6a﹣12b﹣4c+5d)kJmol﹣1
B.﹣(﹣6a+12b+4c﹣5d)kJmol﹣1
C.﹣(﹣4a+6b+4c﹣5d)kJmol﹣1
D.﹣(4a﹣6b﹣4c+5d)kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組物質不屬于同系物的是( ) ①CH2﹣CH﹣COOH和C17H33COOH
② 
③正丁烷和2,2﹣二甲基丙烷
④CH3CH2CHO和 ![]()
A.①③
B.①④
C.②③
D.②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗裝置能達到實驗目的是(夾持儀器未畫出)( )
A. 裝置用于檢驗溴丙烷消去產物
裝置用于檢驗溴丙烷消去產物
B. 裝置用于石油的分餾
裝置用于石油的分餾
C. 裝置用于實驗室制硝基苯
裝置用于實驗室制硝基苯
D. 裝置可裝置證明酸性:鹽酸>碳酸>苯酚
裝置可裝置證明酸性:鹽酸>碳酸>苯酚
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙炔是一種重要的有機化工原料,以乙炔為原料在不同的反應條件下可以轉化成以下化合物. 
完成下列各題:
(1)正四面體烷的分子式為 , 其二氯取代產物有種.
(2)關于乙烯基乙炔分子的說法錯誤的是:; a.能使酸性KMnO4溶液褪色
b.1mol乙烯基乙炔能與3mol Br2發生加成反應
c.乙烯基乙炔分子內含有兩種官能團
d.等質量的乙炔與乙烯基乙炔完全燃燒時的耗氧量不相同
(3)寫出與環辛四烯互為同分異構體且屬于芳香烴的分子的結構簡式 .
(4)寫出與苯互為同系物且一氯代物只有兩種的物質的結構簡式(舉兩例):、 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,不屬于氧化還原反應的是( )
A.H2+F2═2HF
B.3CO+Fe2O3 ![]() ?2Fe+3CO2
?2Fe+3CO2
C.NaOH+HCl═NaCl+H2O
D.4HNO3 ![]() ?2H2O+4NO2↑+O2↑
?2H2O+4NO2↑+O2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘是人體不可缺少的元素,為了防止碘缺乏,現在市場上流行一種加碘鹽,就是在精鹽中添加一定量的KIO3進去.某研究小組為了檢測某加碘鹽中是否含有碘,查閱了有關的資料,發現其檢測原理是:在溶液中 KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)用雙線橋表示該反應中電子轉移的方向和數目:該反應中氧化產物與還原產物的質量比是 , 0.1mol KIO3參加反應時轉移電子mol
(2)實驗結束后分離I2和K2SO4溶液所用的試劑是 A.Na2SO4溶液B.酒精 C. CCl4 D.食鹽水
所用的分離方法是 , 所用儀器是 , 你怎么判斷該食鹽中是否含碘 .
(3)上面實驗中用到一定物質的量濃度的稀硫酸,若配制1mol/L的稀硫酸溶液480mL,需用18mol/L濃H2SO4mL,配制中需要用到的主要玻璃儀器是(填序號) . A.100mL量筒 B.托盤天平 C.玻璃棒D.100mL容量瓶 E.50mL 量筒 F.膠頭滴管 G.燒杯 H.500mL容量瓶
(4)下面操作造成所配稀硫酸溶液濃度偏高的是
A.溶解后溶液沒有冷卻到室溫就轉移
B.轉移時沒有洗滌燒杯、玻璃棒
C.向容量瓶加水定容時眼睛俯視液面
D.用量筒量取濃硫酸后洗滌量筒并把洗滌液轉移到容量瓶
E.搖勻后發現液面低于刻度線,又加蒸餾水至刻度線.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組同學利用氧化還原反應:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O設計如下原電池,鹽橋中裝有飽和溶液.下列說法正確的是( ) 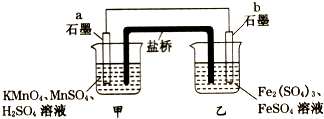
A.a電極上發生的反應為:MnO4﹣+8H++5e﹣═Mn2++4H2O
B.外電路電子的流向是從a到b
C.電池工作時,鹽橋中的SO42﹣移向甲燒杯
D.b電極上發生還原反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com