
【題目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和K+。取該溶液100mL,加入過量NaOH溶液,加熱,得到0.02mol NH3氣體(假設生成氣體完全逸出),同時產生紅褐色沉淀;過濾,洗滌,灼燒,得到1.6g固體(已知難溶性堿受熱易分解,生成相應的金屬氧化和水,如 M(OH)n![]() MOn/2+
MOn/2+![]() H2O)向上述濾液中加足量BaCl2溶液,得到4.66g不溶于鹽酸的沉淀。由此可知原溶液中
H2O)向上述濾液中加足量BaCl2溶液,得到4.66g不溶于鹽酸的沉淀。由此可知原溶液中
A.至少存在3種離子
B.CO32-、K+一定不存在
C.SO42-、NH4+、Fe3+一定存在,Cl-可能不存在
D.Cl- 一定存在
【答案】D
【解析】
加入過量NaOH溶液,加熱,得到0.02mol氣體,可知一定存在NH4+,其物質的量是n(NH4+)=0.02mol,產生的紅褐色沉淀是Fe(OH)3,1.6g固體為Fe2O3,可知一定有Fe3+,由于Fe3+與CO32-會發生反應,所以一定沒有CO32-,n(Fe2O3)=1.6g÷160g/mol=0.01mol,則根據Fe元素守恒可知n(Fe3+)=2n(Fe2O3)=0.02mol;4.66g不溶于鹽酸的沉淀,為BaSO4沉淀,n(BaSO4)=4.66g÷233g/mol=0.02mol,則n(SO42-)=n(BaSO4)= 0.02mol,溶液中存在電荷守恒,NH4+、Fe3+所帶正電荷為3n(Fe3+)+n(NH4+)=3×0.02mol+0.02mol=0.08mol,SO42-所帶負電荷為2n(SO42-)=2×0.02mol=0.04mol,所以溶液中一定存在陰離Cl-離子。
A.由上述分析可知,一定含SO42-、NH4+、Fe3+、Cl-,所以至少存在四種離子,A錯誤;
B.由電荷守恒可知,CO32-一定不存在,K+可能有,也可能沒有,B錯誤;
C.由上述分析可知,一定含SO42-、NH4+、Fe3+、Cl-,C錯誤;
D. 由上述分析可知,一定含Cl-,D正確;
故合理選項是D。


科目:高中化學 來源: 題型:
【題目】在密閉容器中的一定量混合氣體發生反應:x A(g) + y B(g) ![]() z C(g),平衡時測得A的濃度為0.5 mol/L,保持溫度不變,將容器的容積擴大到原來的兩倍,再次達到平衡時,測得A的濃度降低為0.3 mol/L,下列有關判斷正確的是( )
z C(g),平衡時測得A的濃度為0.5 mol/L,保持溫度不變,將容器的容積擴大到原來的兩倍,再次達到平衡時,測得A的濃度降低為0.3 mol/L,下列有關判斷正確的是( )
A.x + y < z B.B的轉化率降低
C.平衡向正反應方向移動 D.C的體積分數增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[物質結構與性質]
高溫煉銅的反應之一為2CuFeS2+O2![]() Cu2S+2FeS+SO2。
Cu2S+2FeS+SO2。
(1) Cu+基態核外電子排布式為________________。

(2) Cu、Zn的第二電離能:I2(Cu)________(填“>”“<”或“=”)I2(Zn)。
(3) SO2分子中S原子的軌道雜化類型為________,分子的空間構型為________,與SO2互為等電子體的分子有________(寫一種)。
(4) [Cu(CH3CN)4]+是非常穩定的絡合離子,配體中σ鍵和π鍵個數之比為________。
(5) Fe2+、Fe3+能與CN-絡合,其結構如圖所示。該離子可形成鐵藍鉀鹽,該鉀鹽的化學式為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】LiH2PO4是制備電池的重要原料。室溫下,LiH2PO4溶液的pH隨c初始(H2PO4–)的變化如圖1所示,H3PO4溶液中H2PO4–的分布分數δ隨pH的變化如圖2所示,[![]() ]下列有關LiH2PO4溶液的敘述正確的是
]下列有關LiH2PO4溶液的敘述正確的是


A. 溶液中存在3個平衡
B. 含P元素的粒子有H2PO4–、HPO42–、PO43–
C. 隨c初始(H2PO4–)增大,溶液的pH明顯變小
D. 用濃度大于1 mol·L-1的H3PO4溶液溶解Li2CO3,當pH達到4.66時,H3PO4幾乎全部轉化為LiH2PO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿式硫酸鐵[Fe(OH)SO4 ]是一種新型高效絮凝劑,常用于污水處理,在醫療上也可用于治療消化性潰瘍出血。工業上利用廢鐵屑(含少量氧化鋁等)生產堿式硫酸鐵的工藝流程如下所示:

部分陽離子以氫氧化物形式沉淀時溶液的pH如表所示:
沉淀物 | Fe(OH) 3 | Fe(OH) 2 | Al(OH) 3 |
開始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
請回答下列問題:
(1)加入少量NaHCO3 的目的是調節溶液的pH,除去Al3+ ,①pH的范圍__________,②寫出可能發生的離子方程式:________________。
(2)在實際生產中,反應Ⅱ中常同時通入O2 ,以減少NaNO2 的用量,O2 與NaNO2 在反應中均作__________。若參與反應的O2 有11.2 L(標準狀況),則相當于節約NaNO2 的物質的量為________。
(3)堿式硫酸鐵溶于水后產生的Fe(OH)2+ 可部分水解生成Fe2(OH)42-,該水解反應的離子方程式為________________________________________________________________。 Fe(OH)3 的Ksp =____________。(提示,開始沉淀c(Fe 3+ )濃度為1.0×10 -5 mol/L)
(4)在醫藥上常用硫酸亞鐵與硫酸、硝酸的混合液反應制備堿式硫酸鐵。根據我國質量標準,產品中不得含有Fe2+ 及NO3-。為檢驗所得的產品中是否含有Fe2+ ,應使用的試劑為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氰化鈉是一種劇毒物質,工業上常用硫代硫酸鈉溶液處理廢水中的氰化鈉。硫代硫酸鈉的工業制備原理為:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2 。某化學興趣小組擬用該原理在實驗室制備硫代硫酸鈉,并檢測氰化鈉廢水處理排放情況。
I.實驗室通過如圖所示裝置制備Na2S2O3
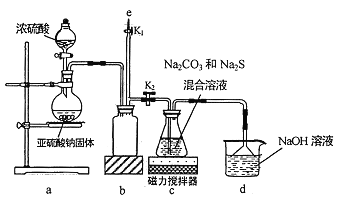
(1)實驗中要控制SO2生成速率,可采取的措施有_____________(寫出一條)。
(2)b裝置的作用是_____________ 。
(3)反應開始后,c 中先有淡黃色渾濁產生,后又變為澄清,此渾濁物為__________(填化學式)。
(4)實驗結束后,在e處最好連接盛__________(填“NaOH 溶液”、“水”、“CCl4”中的一種) 的注射器,接下來的操作為______________,最后拆除裝置。
II.氰化鈉廢水處理
(5)已知: a.廢水中氰化鈉的最高排放標準為0.50mg/L;
b.Ag++2CN-==[Ag(CN)2]-,Ag++I-=AgI↓,AgI 呈黃色,且CN-優先與Ag+反應。
實驗如下: 取20.00mL處理后的氰化鈉廢水于錐形瓶中,并滴加幾滴KI溶液作指示劑,用1.00×10-4mol/L的標準AgNO3溶液滴定,消耗AgNO3溶液的體積為1.50mL。
①滴定時1.00×10-4mol/L的標準AgNO3溶液應用________(填儀器名稱) 盛裝; 滴定終點時的現象是______________。
②處理后的廢水是否達到排放標準_______(填“是”或“否”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,將22.4LHCl完全溶于1L水中(水的密度近似為1g/mL),溶液的密度為ρg/cm3(ρ>1),溶液的體積為VmL,溶質的質量分數為w,溶質的物質的量濃度為c mol/L。下列敘述中正確的是
①w=![]() ×100% ②c=1molL﹣1 ③向上述溶液中再加入VmL水后,所得溶液的質量分數大于0.5w④向上述溶液中再加入VmL水后,所得溶液的質量分數小于0.5w
×100% ②c=1molL﹣1 ③向上述溶液中再加入VmL水后,所得溶液的質量分數大于0.5w④向上述溶液中再加入VmL水后,所得溶液的質量分數小于0.5w
A.①②B.②③C.①③D.①④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二茂鐵可用作燃料的節能消煙劑、抗爆劑等。實驗室制備二茂鐵裝置示意圖如圖

已知:①二茂鐵熔點是173℃,在100℃時開始升華;沸點是249℃。
②制備二茂鐵的反應原理是:2KOH+FeCl2+2C5H6=Fe(C5H5)2+2KCl+2H2O
實驗步驟為:
①在三頸燒瓶中加入25g粉末狀的KOH,并從儀器a中加入60mL無水乙醚到 燒瓶中,充分攪拌,同時通氮氣約l0min;
②再從儀器a滴入5.5mL新蒸餾的環戊二烯(C5H6質量為5.225g),攪拌;
③將足量的無水FeCl2(CH3)2SO(二甲亞砜,作溶劑〕配成的溶液25mL裝入儀器a中,慢慢滴入儀器c中,繼續攪拌45min;
④再從儀器a加入25mL無水乙醚攪拌;
⑤將c中的液體轉入分液漏斗中,依次用鹽酸、水各洗滌兩次,分液得橙黃色溶液;
⑥蒸發橙黃色溶液,得二茂鐵粗產品。
回答下列問題:
(1)儀器b的名稱是______________。
(2)步驟①中通入氮氣的目的是______________。
(3)步驟⑤用鹽酸洗滌的目的是______________。
(4)步驟⑦是二茂鐵粗產品的提純,該過程在下圖中進行,其操作名稱為_____________;該操作中棉花的作用是______________。

(5)為了確認得到的是二茂鐵,還需要進行的一項簡單實驗是_____________________;若最終制得純凈的二茂鐵4.3g,則該實驗的產率為_____________(保留三位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,下列不能用勒夏特列原理解釋的是
A. 合成氨時將氨液化分離,可提高原料的利用率
B. H2、I2、HI 混合氣體加壓后顏色變深
C. 實驗室常用排飽和NaCl溶液的方法收集Cl2
D. 新制氯水中,滴加硝酸銀溶液,溶液顏色變淺
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com