
偏二甲肼與N2O4是常用的火箭推進劑,二者發生如下化學反應:
(CH3)2NNH2 (l)+2N2O4 (l)=2CO2 (g)+3N2(g)+4H2O(g) (I)
(1)反應(I)中氧化劑是_______。
(2)火箭殘骸中常現紅棕色氣體,原因為:N2O4 (g)  2NO2 (g) (Ⅱ) 一定溫度下,反應(Ⅱ)的焓變為ΔH。現將1 mol N2O4 充入一恒壓密閉容器中,下列示意圖正確且能說明反應達到平衡狀態的是________。
2NO2 (g) (Ⅱ) 一定溫度下,反應(Ⅱ)的焓變為ΔH。現將1 mol N2O4 充入一恒壓密閉容器中,下列示意圖正確且能說明反應達到平衡狀態的是________。
若在相同溫度下,上述反應改在體積為1L的恒容密閉容器中進行,平衡常數________(填“增大”“不變”或“減小”),反應3s后NO2的物質的量為0.6mol,則0~3s內的平均反應速率v(N2O4)=________mol·L-1·s-1。
(3)NO2可用氨水吸收生成NH4NO3。25℃時,將amol NH4NO3溶于水,溶液顯酸性,原因是_____
_______________________________________________(用離子方程式表示)。向該溶液滴加bL氨水后溶液呈中性,則滴加氨水的過程中的水的電離平衡將______(填“正向”“不”或“逆向”)移動,所滴加氨水的濃度為_______mol·L-1。(NH3·H2O的電離平衡常數取Kb=2×10-5 mol·L-1,假設溶液的體積是bL)
(每空2分,共14分)(1)N2O4 (2) a、d 不變 0.1
(3)NH4++H2O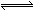 NH3·H2O+H+ 逆向
NH3·H2O+H+ 逆向 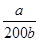
解析試題分析:(1)根據反應(CH3)2NNH2 (l)+2N2O4 (l)=2CO2 (g)+3N2(g)+4H2O(g)可知,(CH3)2NNH2中氮元素的化合價從-2價升高到0價,N2O4中氮元素的化合價從+4價降低到0價,因此氧化劑是N2O4。
(2)在一定條件下,當可逆反應的正反應速率和逆反應速率相等時(但不為0),反應體系中各種物質的濃度或含量不再發生變化的狀態,稱為化學平衡狀態,據此可以判斷。a、密度是混合氣的質量和容器容積的比值,在反應過程中質量不變,但容器容積是變化的,因此當密度不再發生變化時可以說明反應達到平衡狀態,a正確;b、對于具體的化學反應,反應熱是恒定的,不能說明反應達到平衡狀態,b不正確;c、反應物的正反應速率是逐漸減小的,而生成物的正反應速率是逐漸增大,所以c不正確;d、當反應物的轉化率不再發生變化時,說明正逆反應速率相等,達到平衡狀態,d正確,答案選ad;平衡常數只與溫度有關系,所以此時平衡常數不變;反應3s后NO2的物質的量為0.6mol,則根據方程式可知,消耗N2O4的物質的量是0.3mol,其濃度是0.3mol÷1L=0.3mol/L,則0~3s內的平均反應速率v(N2O4)=0.3mol/L÷3s=0.1mol·L-1·s-1。
(3)NH3NO3溶于水電離出的NH4+水解,溶液顯酸性,水解方程式為NH4++H2O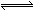 NH3·H2O+H+;氨水是弱堿,電離出的OH-抑制水的電離,所以滴加氨水的過程中的水的電離平衡將逆向移動;溶液顯中性,則根據電荷守恒可知c(NO3-)+c(OH-) =c(NH4+)+c(H+),因此 c(OH-)=c(H+)=10-7mol/L, c(NH4+)=c(NO3-)。根據氨水的電離平衡常數可知,溶液中
NH3·H2O+H+;氨水是弱堿,電離出的OH-抑制水的電離,所以滴加氨水的過程中的水的電離平衡將逆向移動;溶液顯中性,則根據電荷守恒可知c(NO3-)+c(OH-) =c(NH4+)+c(H+),因此 c(OH-)=c(H+)=10-7mol/L, c(NH4+)=c(NO3-)。根據氨水的電離平衡常數可知,溶液中 =2×10-5 mol·L-1,則c(NH3·H2O)=
=2×10-5 mol·L-1,則c(NH3·H2O)=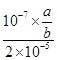 =
=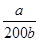 。
。
考點:考查氧化還原反應、平衡狀態判斷、反應速率計算以及鹽類水解、電離平衡常數的計算


科目:高中化學 來源: 題型:填空題
化學在環境保護中起著十分重要的作用。催化反硝化法和電化學降解法可用于治理水中硝酸鹽的污染。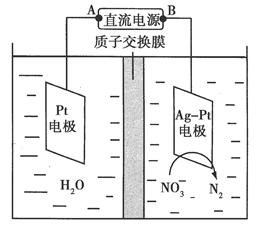
(1)催化反硝化法中,H2能將NO3-還原為N2。25℃時,反應進行10 min,溶液的pH由7變為12。
①N2的結構式為________。
②上述反應離子方程式為____________________,其平均反應速率v(NO3-)為________mol·L-1·min-1。
③還原過程中可生成中間產物NO2-,寫出3種促進NO2-水解的方法________。
(2)電化學降解NO3-的原理如圖所示。
①電源正極為________(填“A”或“B”),陰極反應式為______________。
②若電解過程中轉移了2 mol電子,則膜兩側電解液的質量變化差(Δm左-Δm右)為________g。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
臭氧可用于凈化空氣、飲用水的消毒、處理工業廢物和作漂白劑。
(1)臭氧幾乎可與除鉑、金、銥、氟以外的所有單質反應。如:6Ag(s)+O3(g)=3Ag2O(s) ΔH=-235.8 kJ·mol-1。已知2Ag2O(s)=4Ag(s)+O2(g) ΔH=+62.2 kJ·mol-1,則常溫下反應2O3(g)=3O2(g)的ΔH=________。
(2)配平下面反應的化學方程式(將各物質的化學計量數填在相應的方框內):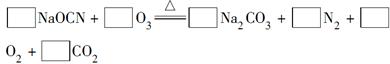
(3)科學家P.Tatapudi等人首先使用在酸性條件下電解水的方法制得臭氧。臭氧在陽極周圍的水中產生,電極反應式為3H2O-6e-=O3↑+6H+,陰極附近溶解在水中的氧氣生成過氧化氫,其電極反應式為_______________________。
(4)空氣中臭氧的檢測方法是將空氣慢慢通過足量KI淀粉溶液,若溶液變藍色,則說明空氣中含有O3。已知O3與KI溶液反應生成兩種單質,則該反應的離子方程式為_____________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
歐盟原定于2012年1月1日起征收航空碳排稅以應對冰川融化和全球變暖,使得對如何降低大氣中CO2的含量及有效地開發利用碳資源的研究顯得更加緊迫。請運用化學反應原理的相關知識研究碳及其化合物的性質。
(1)用電弧法合成的儲氫納米碳管常伴有大量的碳納米顆粒(雜質),這種顆粒可用如下氧化法提純,請完成該反應的化學方程式: 
(2)焦炭可用于制取水煤氣。測得12 g 碳與水蒸氣完全反應生成水煤氣時,吸收了131.6 kJ熱量。該反應的熱化學方程式為 。
(3)活性炭可處理大氣污染物NO。在2 L密閉容器中加入NO和活性炭(無雜質),生成氣體E和F。當溫度分別在T1和T2時,測得各物質平衡時物質的量如下表: 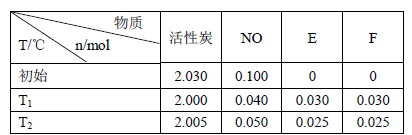
上述反應T1℃時的平衡常數為K1,T2℃時的平衡常數為K2。
Ⅰ.計算K1= 。
Ⅱ.根據上述信息判斷,溫度T1和T2的關系是(填序號) 。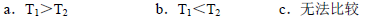
(4)CO2經常用氫氧化鈉來吸收,現有0.4 molCO2,若用200ml 3mol/LNaOH溶液將其完全吸收,溶液中離子濃度由大到小的順序為: 。
(5)CO還可以用做燃料電池的燃料,某熔融鹽燃料電池具有高的發電效率,因而受到重視,該電池用Li2CO3和 Na2CO3的熔融鹽混合物作電解質,CO為負極燃氣,空氣與CO2的混和氣為正極助燃氣,制得在 650 ℃下工作的燃料電池,其負極反應式: 則
則
正極反應式:___ ,電池總反應式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氫化亞銅(CuH)是一種難溶物質,用CuSO4溶液和“另一物質”在40~50℃時反應可生成它。CuH具有的性質有:不穩定,易分解;在氯氣中能燃燒;與稀鹽酸反應能生成氣體;Cu+在酸性條件下發生的反應是:2Cu+=Cu2++Cu。
根據以上信息,結合自己所掌握的化學知識,回答下列問題:
(1)用CuSO4溶液和“另一物質”制CuH的反應中,用氧化還原觀點分析,這“另一物質”在反應中作______(填“氧化劑”或“還原劑”)。
(2)寫出CuH在氯氣中燃燒的化學反應方程式:________________________。
(3)CuH溶解在稀鹽酸中生成的氣體是______(填化學式)。
(4)如果把CuH溶解在足量的稀硝酸中生成的氣體只有NO,請寫出CuH溶解在足量稀硝酸中反應的離子方程式:_____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硝酸是一種強氧化性、腐蝕性的強酸,其還原產物因硝酸濃度的不同而有變化,從總體上說,硝酸濃度越高,平均每分子硝酸得到的電子數越少,濃硝酸的還原產物主要為NO2,稀硝酸的還原產物主要為NO。 實驗室中,常用Cu與濃HNO3反應制取NO2,用Cu與稀HNO3反應制取NO。
(1)請寫出實驗室中用Cu與濃HNO3反應制取NO2的化學方程式:_____________。
(2)該反應中發生氧化反應的物質是__________,1 mol氧化劑_________(填“得到”或“失去”)_______ mol電子。
(3)48.0 g Cu與適量的濃HNO3反應,銅全部作用后,共收集到22.4 L氣體(標準狀況下),反應中消耗HNO3的物質的量可能是( )
A.1.5 mol B.2.0 mol C.2.5 mol D.3.0 mol
(4)實際上硝酸不僅可被還原為NO2或NO,濃度更稀時硝酸還可以被還原為N2O、N2、NH4NO3等。請將3種物質: FeSO4、Fe(NO3)3和Fe2(SO4)3分別填入下面對應的橫線上,組成一個未配平的化學方程式。
HNO3 + ______  ______ + ______ + N2O↑ + H2O
______ + ______ + N2O↑ + H2O
并寫出配平后的離子方程式:_________________________。
(5)硝酸的還原產物NO、NO2、N2O等對環境均有副作用,為了可持續發展,當今社會提出的一個新概念——“綠色化學”,它要求從經濟、環保和技術上設計可行的化學反應,則下列由單質銅制取硝酸銅的方法可行且符合“綠色化學”的是( )
A.Cu  Cu(NO3)2
Cu(NO3)2
B.Cu 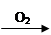 CuO
CuO Cu(NO3)2
Cu(NO3)2
C.Cu 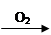 CuO
CuO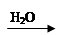 Cu(OH)2
Cu(OH)2 Cu(NO3)2
Cu(NO3)2
D.Cu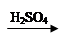 CuSO4
CuSO4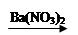 Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
海洋是資源的寶庫,蘊藏著豐富的化學元素,如氯、溴、碘、鎂等。按要求回答下列問題:
(1)可以證明溴比碘的氧化性強的離子反應方程式為____________________________。
(2)從海帶灰中提取的碘單質,往往含有一定的雜質,通常利用加熱的方法除去雜質,這個過程中主要利用碘性質中的___________,也可以通過萃取分液的方法提取碘,實驗室中分液時,分液漏斗中的上層液體應從分液漏斗的_______(填“上”或“下”)口倒出。
(3)點燃的鎂條可以在二氧化碳氣體中繼續燃燒,該反應的化學方程式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
實驗室里通常用MnO2與濃鹽酸反應制取氯氣,其反應的化學方程式為:
MnO2+4HCl(濃)  MnCl2+Cl2↑+ 2H2O
MnCl2+Cl2↑+ 2H2O
(1)在該反應中,如有1 mol Cl2生成,被氧化的HCl的物質的量是 mol,轉移電子的物質的量是 mol。
(2)某溫度下,將Cl2通入NaOH溶液中,反應得到含有ClO-與ClO3-物質的量之比為1∶1的混合液,反應的化學方程式是 。
(3)報紙報道了多起衛生間清洗時,因混合使用“潔廁靈”(主要成分是鹽酸)與“84消毒液”(主要成分是NaClO)發生氯氣中毒的事件。試根據你的化學知識分析,原因是(用離子方程式表示) 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
實驗室里迅速制備少量氯氣可利用以下反應:
KMnO4+ HCl  KCl + MnCl2 + Cl2↑ + H2O
KCl + MnCl2 + Cl2↑ + H2O
(1)請配平上述化學方程式,并在上面用“雙線橋法” 標明電子轉移的方向和數目:
(2)該反應的氧化產物是 ,KMnO4發生 反應。
(3)HCl在上述反應中顯示出來的性質是 。
| A.氧化性 | B.還原性 | C.酸性 | D.堿性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com