
碳和碳的化合物在生產、生活中的應用非常廣泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一種理想,更是一種值得期待的新的生活方式。
(1)將CO2與焦炭作用生成CO,CO可用于煉鐵等。
①已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1= +489.0 kJ/mol
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ/mol
則CO還原Fe2O3的熱化學方程式為 ;
②氯化鈀(PdCl2)溶液常被應用于檢測空氣中微量CO。PdCl2被還原成單質,反應的化學方程式為 ;
(2)將兩個石墨電極插入KOH溶液中,向兩極分別通入C3H8和O2構成丙烷燃料電池。
①負極電極反應式是: ;
②某同學利用丙烷燃料電池設計了一種電解法制取Fe(OH)2的實驗裝置(如下圖所示),通電后,溶液中產生大量的白色沉淀,且較長時間不變色。下列說法中正確的是 (填序號)
A.電源中的a一定為正極,b一定為負極
B.可以用NaCl溶液作為電解液
C.A、B兩端都必須用鐵作電極
D.陰極發生的反應是:2H++2e-=H2↑
(3)將不同量的CO(g)和H2O(g)分別通入體積為2L的恒容密閉容器中,進行反應:CO(g)+H2O(g)  CO2(g)+H2(g),得到如下三組數據:
CO2(g)+H2(g),得到如下三組數據:
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
(1)①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=﹣28.5kJ/mol
②PdCl2+CO+H2O=Pd+CO2+2HCl
(2)①C3H8-20e-+26OH-=3CO32-+17H2O ②BD
(3)① 放熱 ② K=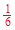 ③使用了催化劑;加大了壓強
③使用了催化劑;加大了壓強
(4)c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
解析試題分析:(1)①將第一個方程式減去3倍的第二個方程式可得目標方程式,反應熱作相應的變化的即可。
②Pd被還原,則CO被氧化為CO2,根據原子守恒還應有H2O參與反應,另一種產物為HCl。
(2)①電池原理是丙烷燃燒,生成的CO2會與KOH反應生成碳酸鹽。燃料電池通入燃料丙烷的一極是負極,因此負極的電極反應式為C3H8-20e-+26OH-=3CO32-+17H2O。
②用電解法制備Fe(OH)2,陽極材料用Fe,電極反應式為Fe-2e-=Fe2+,陰極溶液中的H+放電,電極反應式為2H++2e-=H2↑,電解質可用NaCl溶液。反應產生H2,使生成物處于還原氛圍中,因此A、B兩極都可作陽極。
(3)①實驗2與實驗1相比,各物質的物質的量減少一半,平衡CO2應為0.8mol,但溫度升高,此時CO2的為0.4mol,說明升高溫度平衡逆向移動,逆反應吸熱,則正反應為放熱反應。
②根據題意有:CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
初始量/mol 1 2 0 0
變化量/mol 0.4 0.4 0.4 0.4
平衡量/mol 0.6 1.6 0.4 0.4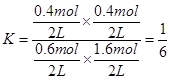
③實驗3與實驗2相比,平衡狀態未變,但反應速率加快,因此改變的條件可能是加入催化劑或增大壓強。
(4)根據題中所給的各物質的物質的量,可知反應后所得的是等物質的量的Na2CO3、NaHCO3的混合溶液,CO32-、HCO3-水解使溶液顯堿性,且CO32-的水解程度大于HCO3-,因此溶液中各離子的物質的量濃度由大到小的順序為c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。
考點:考查蓋斯定律,電解池,電極反應式書寫,影響化學平衡因素,化學平衡常數,鹽的水解等。


科目:高中化學 來源: 題型:填空題
硝酸工業的基礎是氨的催化氧化,在催化劑作用下發生如下反應:
① 4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H =" —905" kJ/mol ①主反應
4NO(g)+6H2O(g) △H =" —905" kJ/mol ①主反應
② 4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H =" —1268" kJ/mol ②副反應
2N2(g)+6H2O(g) △H =" —1268" kJ/mol ②副反應
有關物質產率與溫度的關系如甲圖。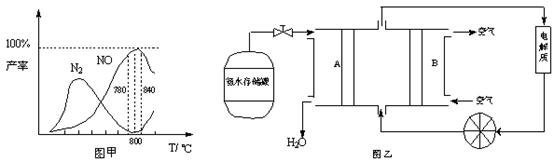
(1)由反應①②可知反應⑤N2(g) + O2(g) 2NO(g)的反應熱ΔH=
2NO(g)的反應熱ΔH=
(2)由圖甲可知工業上氨催化氧化生成 NO時,反應溫度最好控制在
(3)用Fe3O4制備Fe(NO3)3溶液時,需加過量的稀硝酸,原因一:將Fe4O3中的Fe2+全部轉化為Fe3+,
原因二: (用文字和離子方程式說明)。
(4)將NH3通入NaClO溶液中,可生成N2H4,則反應的離子方程式為 。
(5)依據反應②可以設計成直接供氨式堿性燃料電池(如乙圖所示),則圖中A為 (填“正極”或“負極”),電極方程式為
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(15分)(1)25℃時,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。請回答下列問題:
①HA是________(填“強電解質”或“弱電解質”);
②在加水稀釋HA溶液的過程中,隨著水量的增加而減小的是________(填字母)。
A.c(H+)/c(HA) B.c(HA)/(A-) C.c(H+)與c(OH-)的乘積 D.c(OH-)
③若M溶液是由上述HA溶液V1 mL與pH = 12的NaOH溶液V2 mL混合充分反應而得,則下列說法中正確的是
A.若溶液M呈中性,則溶液M中c(H+) + c(OH-) = 2.0×10-7 mol·L-1
B.若V1 =V2 ,則溶液M的pH一定等于7
C.若溶液M呈酸性,V1一定大于V2
D.若溶液M呈堿性,V1一定小于V2
(2)若已知在25℃,AgCl的Ksp = 1.8×10-10,現將足量AgCl分別放入:①100 mL 蒸餾水中;②100 mL 0.2mol·L-1 AgNO3溶液中;③100 mL 0.1mol·L-1 AlCl3溶液中;④100 mL 0.1mol·L-1鹽酸中,充分攪拌后,相同溫度下c(Ag+)由大到小的順序是 (用序號連接)
(3)若1mol SO2(g)氧化為1mol SO3(g)的ΔH =-99kJ·mol-1,單質硫的燃燒熱為296kJ·mol-1,則由S(s)生成3 mol SO3(g)的ΔH =
(4)對于2NO2(g) N2O4(g) ΔH < 0反應,在溫度為T1,T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。則下列說法正確的是 。
N2O4(g) ΔH < 0反應,在溫度為T1,T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。則下列說法正確的是 。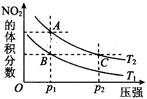
①.A、C兩點的反應速率:A>C
②.A、C兩點氣體的顏色:A深、C淺
③.B、C兩點的氣體的平均分子質量:B<C
④.由狀態B到狀態A,可以用加熱方法
(5)下圖是利用甲烷燃料電池電解50 mL 2 mol·L-1的氯化銅溶液的裝置示意圖: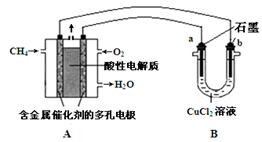
請回答:
① 甲烷燃料電池的負極反應式是 。
② 當線路中有0.2 mol電子通過時,陰極增重____g。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
硼及其化合物在耐髙溫合金工業、催化劑制造、髙能燃料等方面應用廣泛。
(1)氮化硼是一種耐高溫材料,巳知相關反應的熱化學方程式如下:
2B(s)+N2(g)= 2BN(s) ΔH="a" kJ ? mol-1
B2H6 (g)=2B(s) + 3H2 (g) ΔH =b kJ ? mol-1
N2 (g) + 3H2 (g) 2NH3 (g) ΔH ="c" kJ? mol-1
2NH3 (g) ΔH ="c" kJ? mol-1
①反應B2H6(g)+2NH3(g)=2BN(s)+6H2(g) ΔH = (用含a、b、c的代數式表示)kJ ·mol-1。
②B2H6是一種髙能燃料,寫出其與Cl2反應生成兩種氯化物的化學方程式: 。
(2)硼的一些化合物的獨特性質日益受到人們的關注。
①最近美國化學家杰西·薩巴蒂尼發現由碳化硼制作的綠色焰火比傳統焰火(硝酸鋇)更安全,碳化硼中硼的質量分數為78. 6%,則碳化硼的化學式為 。
②近年來人們將LiBH4和LiNH2球磨化合可形成新的化合物Li3BN2H8和Li4BN3 H10,Li3BN2H8球磨是按物質的量之比n(LiNH2) : n(LiBH4) =" 2" : 1加熱球磨形成的,反應過程中的X衍射圖譜如圖所示。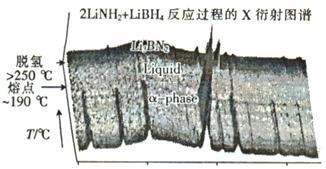
Li3BN2H8在大于250℃時分解的化學方程式為 ,Li3BN2H8與Li4BN3H10的物質的量相同時,充分分解,放出等量的H2,Li4BN3 H10分解時還會產生固體Li2NH和另一種氣體,該氣體是 。
(3)直接硼氫化物燃料電池的原理如圖,負極的電極反應式為 。電池總反應的離子方程式為 。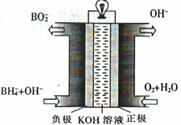
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
化學反應原理在工業生產中具有十分重要的意義。
(1)合成氨用的氫氣有多種制取方法:請你寫出用C制備水煤氣的化學反應方程式 。還可以由天然氣或重油制取氫氣:CH4+H2O(g) 高溫催化劑CO+3H2;比較以上兩種方法轉移6mol電子時,C和CH4的質量之比是 。
(2)工業生產可以用NH3(g)與CO2(g)經過兩步反應生成尿素,兩步反應的能量變化示意圖如下: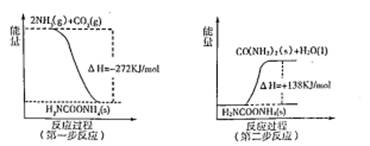
則NH3(g)與CO2(g)反應生成尿素的熱化學方程式為 。
(3)已知反應Fe(s)+CO2(g)=FeO(s)+CO(g) △H=akJ/mol。測得在不同溫度下,該反應的平衡常數K隨溫度的變化如下:
①該反應的化學平衡常數表達式K= ,a 0(填“>”、“<”或“:”)。在500℃2L密閉容器中進行反應,Fe和CO2的起始量均為4 mol,則5min后達到平街時CO2的轉化率為 ,生成CO的平均速率v(CO)為 。
②700℃反應達到平衡后,要使該平衡向右移動,其他條件不變時,可以采取的措施有 (填字母)。
| A.縮小反應器容積 | B.增加Fe的物質的量 |
| C.升高溫度到900℃ | D.使用合適的催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
工業上采用乙苯與CO2脫氫生產重要化工原料苯乙烯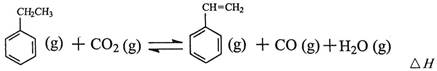
其中乙苯在CO2氣氛中的反應可分兩步進行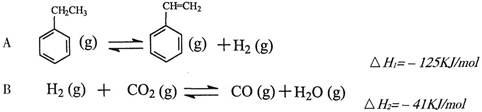
(1)上述乙苯與CO2反應的反應熱△H為________________________。
(2)①乙苯與CO2反應的平衡常數表達式為:K=______________________。
②下列敘述不能說明乙苯與CO2反應已達到平衡狀態的是_____________________。
a.v正(CO)=v逆(CO) b.c(CO2)=c(CO)
c.消耗1mol CO2同時生成1molH2O d.CO2的體積分數保持不變
(3)在3L密閉容器內,乙苯與CO2的反應在三種不同的條件下進行實驗,乙苯、CO2的起始濃度分別為1.0mol/L和3.0mol/L,其中實驗I在T1℃、0.3MPa,而實驗II、III分別改變了實驗其他條件;乙苯的濃度隨時間的變化如圖I所示。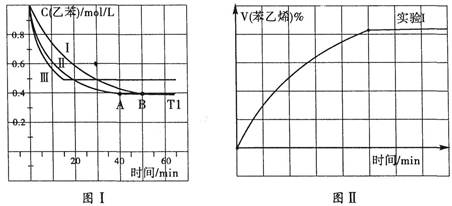
①實驗I乙苯在0~50min時的反應速率為_______________。
②實驗II可能改變條件的是__________________________。
③圖II是實驗I中苯乙烯體積分數V%隨時間t的變化曲線,請在圖II中補畫實驗Ⅲ中苯乙烯體積分數V%隨時間t的變化曲線。
(4)若實驗I中將乙苯的起始濃度改為1.2mol/L,其他條件不變,乙苯的轉化率將(填“增大”、“減小”或“不變”),計算此時平衡常數為_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
)含硫化合物在工業生產中有廣泛的用途。
(1)SO2可用于工業生產SO3。
①在一定條件下,每生成8g SO3氣體,放熱9.83kJ。該反應的熱化學方程式為__________________
②在500℃,催化劑存在的條件下,向容積為1L的甲、乙兩個密閉容器中均充入2 mol SO2和1 mol O2。甲保持壓強不變,乙保持容積不變,充分反應后均達到平衡。
I.平衡時,兩容器中SO3體積分數的關系為:甲_______乙(填“>”、“<”或“ =”)。
II.若乙在t1 min時達到平衡,此時測得容器乙中SO2的轉化率為90%,則該反應的平衡常數為_______;保持溫度不變,t2 min時再向該容器中充入1 mol SO2和1 mol SO3,t3 min時達到新平衡。請在下圖中畫出t2~t4min內正逆反應速率的變化曲線(曲線上必須標明V正、 V逆)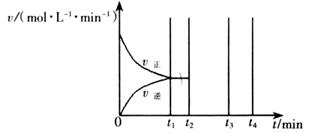
(2)硫酸鎂晶體(MgSO4·7H2O )在制革、醫藥等領域均有廣泛用途。4.92g硫酸鎂晶體受熱脫水過程的熱重曲線(固體質量隨溫度變化的曲線)如右圖所示。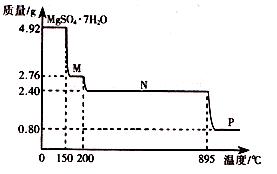
①固體M的化學式為__________。
②硫酸鎂晶體受熱失去結晶水的過程分為_________個階段。
③N轉化成P時,同時生成另一種氧化物,該反應的化學方程式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
利用如圖所示裝置測定中和熱的實驗步驟如下: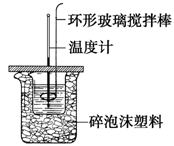
步驟一:用量筒量取50ml 0.50 mol?L-1鹽酸倒入小燒杯中,測出鹽酸溫度t1;
步驟二:用另一量筒量取50ml 0.55 mol?L-1 NaOH溶液,并用另一溫度計測出其溫度t2;
步驟三:將NaOH溶液倒入小燒杯中,設法使之混合均勻,測得混合液最高溫度t3。
回答下列問題:
(1)步驟三中倒入NaOH溶液的正確操作是__________。
A.沿玻璃棒緩慢倒入 B.分三次少量倒入 C.一次迅速倒入
(2)使鹽酸與NaOH溶液混合均勻的正確操作是________(填序號)。
A.輕輕地振蕩燒杯 B.揭開硬紙片用玻璃棒攪拌
C.用溫度計小心攪拌 D.用套在溫度計上的環形玻璃攪拌棒輕輕地攪動
(3)___________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替NaOH溶液和鹽酸測中和熱,理由是________________________________________。
(4)在反應中若因為有放熱現象,而造成少量HCl在反應中揮發,則測得的中和熱_______(填“偏大”、“偏小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
t℃時,在體積不變的容器中發生反應X(g)+3Y(g) 2Z(g)△H<O各組分濃度如下表
2Z(g)△H<O各組分濃度如下表
| 物質 | X | Y | Z |
| 初始濃度/ mol·L-1 | 0.1 | 0.3 | 0 |
| 2min末濃度/mol·L-1 | 0.08 | | |
| 平衡濃度/mol·L-1 | | | 0.1 |
 逆堿小,平衡正向移動
逆堿小,平衡正向移動查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com