
(14分)氫能是重要的新能源。儲氫作為氫能利用的關鍵技術,是當前關注的熱點之一。
(1)氫氣是清潔能源,其燃燒產物為__________。
(2)NaBH4是一種重要的儲氫載體,能與水反應達到NaBO2,且反應前后B的化合價不變,該反應的化學方程式為___________,反應消耗1mol NaBH4時轉移的電子數目為__________。
(3)儲氫還可借助有機物,如利用環己烷和苯之間的可逆反應來實現脫氫和加氫: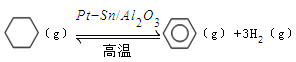 。某溫度下,向恒容密閉容器中加入環己烷,起始濃度為a mol/L,平衡時苯的濃度為bmol/L,該反應的平衡常數K=_____。
。某溫度下,向恒容密閉容器中加入環己烷,起始濃度為a mol/L,平衡時苯的濃度為bmol/L,該反應的平衡常數K=_____。
(4)一定條件下,題11圖示裝置可實現有機物的電化學儲氫(忽略其它有機物)。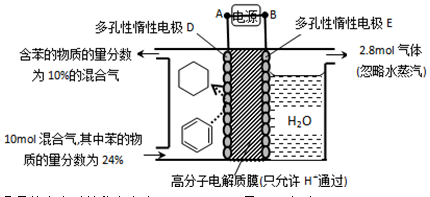
①導線中電子移動方向為____________。
②生成目標產物的電極反應式為_________。
③該儲氫裝置的電流效率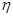 =_____(
=_____(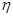 =
= ×100%,計算結果保留小數點后1位)
×100%,計算結果保留小數點后1位)
(1)水或H2O (2)NaBH4+2H2O=NaBO2+4H2↑;4NA或2.408×1024
(3)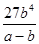 mol3/L3 (4)①A→D ②C6H6+6H++6e-=C6H12 ③64.3%
mol3/L3 (4)①A→D ②C6H6+6H++6e-=C6H12 ③64.3%
解析試題分析:(1)氫氣的燃燒產物是水。
(2)反應前后B元素的化合價不變,則反應前后B元素的化合價均是+3價,因此反應前NaBH4中氫元素的化合價是-1價。水中氫元素的化合價是+1價,因此反應中還有氫氣生成,則反應的化學方程式為NaBH4+2H2O=NaBO2+4H2↑。NaBH4中氫元素的化合價從-1價升高到0價,因此1molNaBH4在反應中失去4mol電子,其數目是4NA或2.408×1024。
(3)平衡時苯的濃度是b mol/L,則根據反應的方程式可知消耗環戊烷的濃度是b mol/L,生成氫氣的濃度是3 b mol/L,,平衡時環戊烷的濃度為(a-b)mol/L。由于化學平衡常數是在一定條件下,當可逆反應達到平衡狀態時,生成物濃度的冪之積和反應物濃度的冪之積的比值,則該溫度下反應的平衡常數為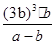 =
=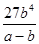 mol3/L3。
mol3/L3。
(4)①苯生成環戊烷屬于得氫反應,因此是還原反應,即電極D是陰極,電極E是陽極,因此導線中電子的流動方向是A→D。
②苯得到電子生成環戊烷是目標產物,由于存在質子交換膜,所以氫離子向陰極移動,則電極反應式為C6H6+6H++6e-=C6H12。
③陽極生成2.8mol氣體,該氣體應該是陽極OH-放電生成的氧氣,則轉移電子的物質的量=2.8mol×4=11.2mol。設陰極消耗苯的物質的量是xmol,則同時生成 xmol環戊烷,根據電極反應式C6H6+6H++6e-=C6H12可知得到電子是6xmol,根據電子守恒可知,陰極生成氫氣是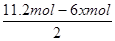 =5.6mol-3xmol,所以
=5.6mol-3xmol,所以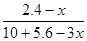 =0.1,解得x=1.2,因此儲氫裝置的電流效率=
=0.1,解得x=1.2,因此儲氫裝置的電流效率= ×100%=64.3%。
×100%=64.3%。
考點:考查氧化還原反應方程式配平和計算、平衡常數計算以及電化學原理的應用與計算


科目:高中化學 來源: 題型:填空題
(8分)(1)氫是未來最好的能源選擇,制取氫氣的成熟的方法有很多,利用甲醇可以與水蒸氣反應生成氫氣,反應方程式如下:
CH3OH(g) + H2O(g)  CO2(g) + 3H2(g)
CO2(g) + 3H2(g) 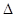 H(298K)=+ 49.4 kJ/mol
H(298K)=+ 49.4 kJ/mol
一定條件下,向容積為2L的恒容密閉容器中充入1 mol CH3OH(g)和3 mol H2O(g),實驗測得:達到平衡狀態時,吸收熱量19.76 kJ。則
①達平衡時混合氣體的壓強是反應前的 倍。
②該條件下的該反應的平衡常數是 (結果保留兩位有效數字)。
③該條件下反應達平衡狀態的依據是(填序號) 。
| A.v正(CH3OH)=v正(CO2) | B.混合氣體的密度不變 |
| C.c(CH3OH)=c(H2O) | D.混合氣體的總物質的量不變 |
 2SO3(g)
2SO3(g) 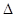 H<0,甲、乙起始反應溫度相同,均和外界無熱量交換,平衡時,甲中SO2的轉化率為a,乙中SO3的分解率為b,則a、b的關系為a+b _______ 1(填“﹤”、“﹥”或“=”) 。
H<0,甲、乙起始反應溫度相同,均和外界無熱量交換,平衡時,甲中SO2的轉化率為a,乙中SO3的分解率為b,則a、b的關系為a+b _______ 1(填“﹤”、“﹥”或“=”) 。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(12分)科學家一直致力于“人工固氮”的方法研究。
(1)合成氨的原理為:N2(g)+3H2(g)  2NH3(g)
2NH3(g)  H="-92.4" kJ/mol,該反應的能量變化如圖所示。
H="-92.4" kJ/mol,該反應的能量變化如圖所示。
①在反應體系中加入催化劑,反應速率增大,E2的變化是 (填“增大”、“減小”或“不變”)。
②將0.3 mol N2和0.5 mol H2充入體積不變的密閉容器中,在一定條件下達到平衡,測得容器內氣體壓強變為原來的 ,此時H2的轉化率為 (計算出結果);欲提高該容器中H2的轉化率,下列措施可行的是 (填選項字母)。
,此時H2的轉化率為 (計算出結果);欲提高該容器中H2的轉化率,下列措施可行的是 (填選項字母)。
| A.向容器中按原比例再充入原料氣 | B.向容器中再充入一定量H2 |
| C.改變反應的催化劑 | D.液化生成物分離出氨 |
 4NH3(g)+3O2(g)
4NH3(g)+3O2(g)  H="+1530" kJ/mol
H="+1530" kJ/mol H="+44.0" kJ/mol
H="+44.0" kJ/mol 4NH3(g)+3O2(g)
4NH3(g)+3O2(g)  H = kJ/mol,該反應的化學平衡常數表達式為K= ,控制其他條件不變,增大壓強,K值 (填“增大”、“減小”或“不變”)。
H = kJ/mol,該反應的化學平衡常數表達式為K= ,控制其他條件不變,增大壓強,K值 (填“增大”、“減小”或“不變”)。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(14分)加大對煤燃燒產生的廢氣、廢渣的處理已刻不容緩。
(1) 對燃煤的廢氣進行脫硝處理時,可利用甲烷催化還原氮氧化物,如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH=a kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH=b kJ·mol-1
則反應CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g)的ΔH=________ kJ·mol-1(用含a、b的代數式表示)。
(2) 將燃煤廢氣中的CO2轉化為二甲醚的反應原理為:
2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g);ΔH
CH3OCH3(g)+3H2O(g);ΔH
① 該反應平衡常數表達式為K=________。
② 已知在某壓強下,該反應在不同溫度、不同投料比時,CO2的轉化率如右圖所示。該反應的ΔH________(填“>”“<”或“=”)0。若溫度不變,減小反應投料比[n(H2) /n(CO2)],則K將________(填“增大”“減小”或“不變”)。
③ 二甲醚燃料電池具有啟動快,效率高等優點,若電解質為酸性,二甲醚燃料電池的負極反應為____________________________。
(3) 以CO2為原料合成的碳酸酯(僅含碳、氫、氧三種元素)是用途廣泛的化學品,某種碳酸酯(DPC)水解產物之一遇氯化鐵溶液顯紫色,右圖為它的核磁共振氫譜圖,請寫出DPC的結構簡式:____________。
(4) 某電廠的粉煤灰含莫來石(主要成分為Al6Si2O13、SiO2)。將其和純堿在高溫下燒結,可制取NaAlSiO4(霞石)、Na2SiO3和NaAlO2,有關化學方程式(反應條件均為高溫)為:
Al6Si2O13+3Na2CO3===2NaAlSiO4+4NaAlO2+3CO2↑
Al6Si2O13+5Na2CO3===2Na2SiO3+6NaAlO2+5CO2↑
SiO2+Na2CO3===Na2SiO3+CO2↑
則用1 mol Al6Si2O13和4 mol SiO2通過以上反應制得5 mol NaAlO2,共消耗Na2CO3為________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(15分)鐵及其化合物與生產、生活關系密切。
(1)下圖是實驗室研究海水對鐵閘不同部位腐蝕情況的剖面示意圖。
①該電化腐蝕稱為 。
②圖中A、B、C、D四個區域,生成鐵銹最多的是 (填字母)。
(2)用廢鐵皮制取鐵紅(Fe2O3)的部分流程示意圖如下:
①步驟I若溫度過高,將導致硝酸分解。硝酸分解的化學方程式為 。
②步驟Ⅱ中發生反應:4Fe(NO3)2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反應產生的HNO3又將廢鐵皮中的鐵轉化為Fe(NO3)2,該反應的化學方程式為 。
③上述生產流程中,能體現“綠色化學”思想的是 (任寫一項)。
(3)已知t℃時,反應FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常數K=0.25。
Fe(s)+CO2(g)的平衡常數K=0.25。
①t℃時,反應達到平衡時n(CO):n(CO2)= 。
②若在1 L密閉容器中加入0.02 mol FeO(s),并通入xmolCO,t℃時反應達到平衡。此時FeO(s)轉化率為50%,則x= 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(17分)H2O2是一種強氧化劑,被廣泛應用于水處理及衛生消毒等方面。
(1)H2O2不穩定,當其中含Fe2+時,會發生反應: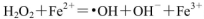
 ,則Fe2+在此過程中所起的作用是______________,當生成336mL O2(標準狀況)時,反應中轉移電子的物質的量為_______mol。
,則Fe2+在此過程中所起的作用是______________,當生成336mL O2(標準狀況)時,反應中轉移電子的物質的量為_______mol。
(2)下表是在常壓、60℃和不同pH條件下,6mL30% H2O2在60min內釋放出氧氣的體積。則下列說法正確的是___________。
a.pH越大,H2O2的分解速率越大
b.pH在9左右,H2O2的分解速率最大
c.6mL 30% H2O2分解最多釋放出的氧氣的體積為639mL
d. pH=5.50時,0~60min內,v(O2)=1.5mL
(3)溶液中H2O2的殘留量可用一定濃度的酸性KMnO4溶液來測定,反應中MnO4-
被還原為Mn2+,該反應的離子方程式為______________。
(4)科學工作者以Ir-Ru/Ti為陽極、ACFC為陰極,在酸性環境、不斷通入空氣的條件下直接電解水來制備H2O2。電解過程中,陽極區溶液的pH_ (填“增大”“不變”或“減小”),陰極產生H2O2的電極反應式為_______。若不通空氣,則陰極得到的產物是_______ 。
(5)己知斷裂1mol化學鍵所需的能量
143,H-O為463。則 .
.
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫酸的消費量是衡量一個國家化工生產水平的重要標志。
(1)一定條件下,SO2與空氣反應10 min后,SO2和SO3物質的量濃度分別為1.2 mol/L和2.0 mol/L,則SO2起始物質的量濃度為______;生成SO3的化學反應速率為______。
(2)若改變外界條件,發生SO2與空氣反應生成SO3,使10 min內的用O2表示的反應速率為0.15mol/(L·min),則改變的條件可能是_______________。
| A.壓縮體積,增大壓強 | B.降低溫度 | C.充入大量的氮氣 | D.僅增加SO2的濃度 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(10分,每空2分) 往一個容積為5L的密閉容器中,通入2molN2和3molH2,在一定條件下,發生反應 N2+3H2 2NH3,2 min后測得容器中生成了1mol NH3,試求:
2NH3,2 min后測得容器中生成了1mol NH3,試求:
(1)2 min時,N2的物質的量 ; (2)2 min時,H2的物質的量濃度 ;
(3)2 min時,H2的轉化率 ; (4)2min內,N2的平均反應速率 ;
(5)N2、H2、NH3的反應速率之比 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
反應A(g) 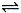 B(g) +C(g)在容積為1.0L的密閉容器中進行,A的初始濃度為0.050mol/L。溫度T1和T2下A的濃度與時間關系如圖所示。回答下列問題:
B(g) +C(g)在容積為1.0L的密閉容器中進行,A的初始濃度為0.050mol/L。溫度T1和T2下A的濃度與時間關系如圖所示。回答下列問題: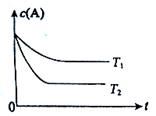
(1)上述反應的溫度T1 T2,平衡常數K(T1) K(T2)。(填“大于”、“小于”或“等于”)
(2)若溫度T2時,5min后反應達到平衡,A的轉化率為70%,則:
①平衡時體系總的物質的量為 。
②反應的平衡常數K= 。
③反應在0~5min區間的平均反應速率v(A)= 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com